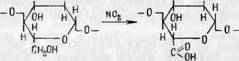
Двуокись азота является более или менее специфическим реагентом,, способным окислять первичные гидроксильные группы целлюлозы до карбоксильных
|
Н ОН
|
|
Н он |
Продукт реакции носит название монокарбоксилцеллюлозы и имеет в настоящее время промышленное значение.
В 1945 г. в США начал работать завод большой производительности по выпуску целлюлозы, окисленной двуокисью азота [16]. Этот продукт является хорошим кровоостанавливающим веществом, способным рассасываться в тканях без анафилактических реакций организма.[20] Он находит и другие применения в медицине, например, в качестве адсорбционного носителя при введении лекарственных веществ; используется как фильтр для сигарет, все шире внедряется в текстильной н других отраслях промышленности.
Окисление целлюлозы может производиться действием на нее газообразной двуокиси азота (N02), жидкого азотноватого ангидрида (N204) или раствора азотноватого ангидрида в индифферентном органическом растворителе (например, в четыреххлористом углероде). Степень окисления целлюлозы обусловливается продолжительностью окисления, температурой и количеством двуокиси азота. Исследуя окисление целлюлозы двуокисью азота в четыреххлористом углероде, Паркинсон показал [18], что реакция протекает предпочтительно в доступных (аморфных) областях целлюлозы.
Окисление целлюлозы двуокисью азота не является, однако, сугубо специфической реакцией первичных гидроксильных групп.
Исследования Каверзневой f19’13] показали, что окисление целлюлозы двуокисью азота всегда сопровождается окислением вторичных гидроксилов. Целлюлозы, окисленные N02, по данным Каверзневой, содержат большое количество карбонильных групп (до 19 групп на 100 глюкозных остатков при 65 карбоксильных группах). В свеже — окисленных препаратах основная масса карбонильных групп является кетонными, в то время как содержание альдегидных групп ничтожно мало (не более 0.3 группы на 100 глюкозных остатков).
Для объяснения механизма окисления целлюлозы окислами азота предложено несколько схем.
В 1947 г. Кешионом и др. [20] была предложена следующая схема окисления целлюлозы
2N204+H20 2HN03 + N203; (С6Н10Ов)я + 7гНГЮз (CeH90N02)B + nH20;
(CbH90N02)„ (CsH8COOH)„.
1и
Эта схема совершенно не учитывает роли окиси азота и N2Os, она не может объяснить ускоряющего действия NO на окисление при известном содержании его в газах, a N203, по Кениону, тормозит эту реакцию.
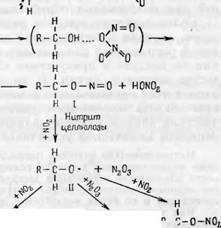
Гораздо лучше согласуется с экспериментальными данными схема окисления целлюлозы N204, предложенная Павлюченко и Ермоленко [9] с поправками Каверзневой и Саловой [21], которая имеет следующий вид
TOC o "1-3" h z Павлюченко, Ермоленко и Каиуц — кии [9 ] путем изучения ультрафиолете — Н
Вых спектров поглощения целлюлоз, п_р_пц + n=N-0—N___ »
Окисленных двуокисью азота, показали, —
Что на первых стадиях реакции образуются легко разрушающиеся при действии влаги нестойкие эфиры азотистой кислоты (нитриты целлюлозы), а не нитраты, как полагал Кенион. В развитие существующих представлений о радикальном механизме действия N204 на углеводороды эти авторы считают, что образовавшийся на первой стадии реакции нитрит (I) распадается на радикал (ii), который может стабилизироваться, окисляясь в карбонильную (iii) и далее карбоксильную (iv) группы за счет N304. С другой стороны, этот радикал может при действии N204 перейти в нитроэфир (v). Таким образом, основная реакция окисления идет через стадию нитрита (I) и его окислительного превращения, а образование нитроэфирных,0 ‘
Групп рассматривается как следствие " LH ‘ <иг п н г,,и ^ побочной реакции. ш у^ Н „
Каверзнева и Салова [21] поддер — о-г*®
Живают в основном схему Павлюченко ч0н
И Ермоленко. Кроме того, они отразили V
В этой схеме участие в реакции N203,
Сделав теоретически вполне обоснованное предположение, что стабилизация радикалов ИСН20 • может происходить не только под влиянием N204, но и N203(N0), и что скорость стабилизации при помощи N203 больше таковой для N204. Если скорость стабилизации радикала КСН20 • под влиянием N203 больше, чем под влиянием N204, то примесь N203 будет ускорять окисление. Такое ускоряющее действие Каверз — знева и Салова нашли при содержании N0, равном 7—10% от суммы окислов.
С другой стороны, возможно, что образовавшиеся в результате побочной реакции нитроэфирные группы подвергаются дальнейшему окислительному расщеплению под влиянием N204 и HN03, как это предполагал Кенион.
Монокарбоксилцеллюлоза является более сильной кислотой, чем уксусная кислота; на вытеснении монокарбоксилцеллюлозой уксусной кислоты из ее солей основан, как уже говорилось, один из методов определения содержания карбоксильных групп.
Окисление первичных гидроксильных групп до карбоксильных даже в небольшом числе элементарных звеньев макромолекулы целлюлозы значительно изменяет свойства получаемых препаратов — изменяется отношение целлюлозы к красителям, медноаммиачная вязкость целлюлозы, ее устойчивость к действию щелочей, кислот и воды при повышенной температуре, а также ухудшается растворимость ее эфиров. В отличие от неокисленной целлюлозы, хорошо окрашиваемой субстантивными красителями (прямой чисто-голубой), монокарбоксилцеллюлоза, содержащая всего 2% карбоксильных групп, уже не окрашивается ими. Обратная картина наблюдается по отношению к основным красителям: в то время как неокисленная целлюлоза почти не окрашивается этими красителями, монокарбоксилцеллюлоза, содержащая всего 2—3% карбоксильных групп, уже способна интенсивно окрашиваться.
Как показали Роговин и др. [10- стр — 292], наличие небольших количеств карбоксильных групп у шестого углеродного атома в цепях целлюлозы
резко понижает устойчивость целлюлозы к действию щелочей и даже воды при повышенной температуре. После кипячения с дистиллированной водой прочная хлопчатобумажная ткань, содержавшая 2—3% карбоксильных групп, полностью рассыпалась в порошок. При введении в целлюлозу такого же количества карбоксилов у второго и третьего углеродных атомов (дикарбоксилцеллюлоза) крепость целлюлозных тканей при аналогичных обработках заметно не менялась.
Более детально вопросы распада целлюлозы, окисленной двуокисью азота, изучали Каверзнева и Кисть [22|. Они показали, что главной причиной распада этой целлюлозы в щелочной среде, так же как и при хранении на воздухе в присутствии влаги, является наличие большого количества кетонных групп. В то же время ускоренный гидролитический распад этих оксицеллюлоз в кислой среде объясняется, вероятно, в первую очередь нарушением упорядоченности межмолекулярного взаимодействия новыми функциональными группами и, в меньшей степени, изменением химической устойчивости цепи макромолекул этими группами.
Медноаммиачная вязкость целлюлозы, окисленной двуокисью азота, значительно ниже медноаммиачной вязкости исходной целлюлозы. Падение медноаммиачной вязкости объясняется в основном деструкцией окисленной целлюлозы при действии на нее медноаммиачного раствора. Однако в некоторой степени деструкция целлюлозы происходит и во время воздействия двуокиси азота на целлюлозу [18].
Как уже отмечалось, окисление даже небольшого количества первичных гидроксильных групп целлюлозы до карбоксильных снижает скорость ее этерификации и ухудшает растворимость полученных эфиров в обычных растворителях. В то же время, как указывает Роговин [2® ], введенне небольших количеств карбоксильных групп в молекулу вискозного и хлопкового корда должно повысить адгезию этих материалов к каучуку, содержащему основные группы, что представляет большой практический интерес.
Благодаря наличию в макромолекуле СООН-групп монокарбоксилцеллюлоза может служить исходным продуктом для синтеза целого ряда производных целлюлозы [23].
Кроме того, образование в ходе окисления целлюлозы двуокисью азота макрорадикалов открывает возможность использования этих макрорадикалов для синтеза новых производных целлюлозы. Так, Ермоленко и Капуцкому [24 J путем обработки целлюлозы, растворенной в фосфорной кислоте, двуокисью азота удалось ввести в макромолекулу целлюлозы до 2—3% химически связанного фосфора, что увеличивает огнестойкость целлюлозы и улучшает ее. ионообменные свойства.

 Опубликовано в рубрике
Опубликовано в рубрике