Как уже говорилось выше, продукты алкилирования лигнина, в особенности метилированный лигнин, очень часто изучались с целью определения числа и природы гидроксильных групп лигнина. Определения, произведенные разными авторами, дают несравнимые результаты даже для одной и той же древесной породы, если лигнин извлечен из нее разными методами.
Браунсом и Льюисом [88] был разработан довольно практический ■процесс приготовления разнообразных простых эфиров лигнина методом алкилирования. В качестве исходного продукта авторы применяли так называемый «мидол», т. е. щелочной лигнин, осажденный углекислотой из отработанных черных щелоков при натронном способе производства целлюлозы из лиственной древесины [89]. Раствор мидола сперва обрабатывали нейтральным или основным ацетатом свинца для осаждения «свинцовой соли» лигнина, на которую затем действовали галоидными алкилами. Указанным способом были получены метиловый, пропиловый, бутиловый, амиловый, бензиловый, стеариловый и другие простые эфиры щелочного лигнина лиственных пород. Как общее правило, йодистые алкилы оказались более реакционноспособными, чем бромиды. Галоидалкилы с короткими цепями были более реакционноспособными, чем с длинными цепями. Стеарилбромид, например, реагирует при 210° в течение 5—6 час., стеа — рилиодид легко реагирует уже при 180°. Нельзя не отметить, что указы
ваемые автором высокие температуры несомненно должны вызывать очень значительные изменения лигнина во время этерификации.
Ацилированпе лигнина также применялось различными авторами для определения активных гидроксильных групп. Ацетилирование производится обычно смесью уксусного ангидрида и пиридина. Кроме ацетильных производных лигнина, ряд авторов получал бензоильные производные и некоторые другие сложные эфиры лигнина.
Брауне и Льюис для получения сложных эфиров также использовали свинцовую соль мидола [88] и получили эфиры лигнина лиственных пород с пропионовой, масляной, бензойной и стеариновой кислотами. Этимв авторами были приготовлены другие металлические производные лигнина и использованы для синтеза его сложных эфиров. Получение сложных эфиров производилось путем нагревания с обратным холодильником суспензии металлического производного в дноксане с галоидангидридом. При этом перешедший в раствор сложный эфир лигнина осаждался прибавлением эфира или воды. Было найдено, что для низших представителей ряда жирных кислот три ацильные группы реагируют с одной основной единицей лигнина с М=840. С увеличением длины цепи ацильного радикала глубина ацилирования понижается.
Н. И. Никитин и Руднева 1®°] получили при действии монохлоруксусной кислоты на лигнин, выделенный солянокислым методом, соответствующий сложный эфир. Реакция происходит при 100—120° с растворением лигнина в избытке реагента в течение нескольких часов. Горячий раствор отфильтровывался, продукт высаживался из фильтрата большим количеством серного эфира и очищался.
При действии монохлоруксусной кислоты непосредственно на древесину ели в раствор переходит не менее двух третей это р иф иди рои апного лигнина с частью углеводов. В этом лигнине оказываются этерифициро — ванными почти три четверти всех гидроксильных групп.
Продукты сплавления лигнина со щелочью.
Теория строения Фрейденберга
Еще в конце прошлого столетия было выяснено, что при сплавлении лигнина с 60—70%-м едким кали при температуре 240—295° можно получить некоторые количества протокатеховой кислоты (9—10% из лигнина хвойной древесины) и пирокатехина
СООН I
Уон он
Протокатеховая кислота
|
У4 ОН ОН Пирокатехин |
Позднее (в 1928 г.) Фрейденберг [91], предположив, что протокатеховая кислота и пирокатехин частично разрушаются при этом процессе и извлекаются с неполным выходом, разработал несколько другой метод количественного определения продуктов щелочной плавки лигнина. Во-первых, Фрейденберг снизил температуру сплавления с 70%-м едким кали до 170—210°. Кроме того, продукты щелочного сплавления, имевшие
Фенольный характер, он подвергал исчерпывающему метилированию* диазометаном и диметилсульфатом, а затем осторожному окислению пер — манганатом калия. Метилирование защищало нестойкие фенольные группировки от последующего окисления. Используя этот метод, Фрейденберг получил из медноаммиачного лигнина ели около 14% вератровой кислоты,, 4% изогемипиновой кислоты и 3% кислоты дегидродивератровой, образующейся вторично в результате конденсации вератровой кислоты СООН СООН СООН СООН
I I II
Нвос/у^оснз
ОСН3
|
Уосн3 0СН3 Вератровая кислота |
Изогемипиновая кислота
|
V�CH, |
ОСНо
Дегидродивератровая кислота
Общее количество полученных ароматических кислот составляло около 20%. Но это количество далеко не покрывало веса всего взятого лигнина. Фрейденберг предположил, что в процессе сплавления со щелочью и последующего метилирования и окисления продуктов выход вератровой и изогемипиновой кислот получался неполный вследствие их частичного окисления и разрушения.
В дальнейших опытах Фрейденберг еще снизил температуру сплавления до 165—170° и в качестве исходного материала взял предварительно, метилированную диазометаном и диметилсульфатом еловую древесину. После сплавления опилок со щелочью проводилось окисление продуктов:, сплавления перманганатом калия. Этим были достигнуты более высокие выходы ароматических кислот. В пересчете на лигнин ели получалось: вератровой кислоты 20%, изогемипиновой кислоты 6—12% и дегидродивератровой 4%, т. е. всего до 36% ароматических кислот к весу лигнина. Фрейденберг считал, что и в этих условиях значительная часть кислот все же разрушалась, особенно изогемипиновая кислота. Фрейденберг склонялся даже к далеко идущему предположению, что истинный выход, изогемипиновой кислоты должен составлять для лигнина хвойных около 80%, так как особые опыты показали, что выход ее составляет от 1/е до 1/10 по сравнению с теоретическим.
Получение подобных продуктов при сплавлении лигнина со щелочыо с последующим метилированием и окислением привело Фрейденберга [<j2J к следующей схеме строения лигнина. Из его выводов следует, что лигнин представляет собой смесь продуктов конденсации, в основе которых лежат следующие простейшие вещества, являющиеся производным». 3,4-диоксифенил пропана
|
Сн2он |
СНО |
СНз |
|
J СНОН |
1 Сн2 |
1 Со |
|
1 СНОН |
1 СНОП |
1 СИОН 1 |
|
1 |
П |
1 1 II |
|
Уосн3 он |
Уосн3 Он |
1 II Уоси он |
|
И |
|
Hi |
В биохимическом процессе синтеза лигнина из этих основных •образуются цепи примерно из 6—7 звеньев за счет простых эфирных связей по типу IV. По мнению автора, вещество III является главнейшей составной частью лигнина, оно лежит в основе примерно 2/3 лигнина. Лигнин такого строения (типа IV) Фрейденберг называл «несформироваи- гаимся» и считал, что он содернсится в молодой древесине. При достижении зрелости древесины, а также при длительном ее хранении или воздействии на пее сильных реагентов (например, крепких кислот) происходит дополнительная конденсация лигнина с образованием в нем единого углеродного скелета. Таким путем образуется «сформировавшийся» лигнин типа V
СН3 | ||
СО УЧОСН3
I I d
|
Сн3 I/W)CH3 С'(он) | Сн—о I |
СН—о
I
Сн„
|
Сн3 | I/Voch, С(ОН) |
|
Со I Сн—о I |
|
VV)ch, |
|
СН — I |
|
О |
|
У�сн3 — О |
|
/уосн3 —О |
Iv
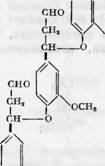
Подобным^же’образом вещество II или I может сперва конденсироваться с образованием только простых эфирных связей типа VI или VIII. При окончательном формировании лигнина происходит до — •полнительная.’жонденсация с образованием лигнина типа VII или IX.
СН(ОН)|
Сн, о
Бн
|
Осн, |
А
Сн(он)|
|
|
|
Осн. |
Сн, о
—о
|
Осн3 |
|
|
|
Осн. |
|
Осн3 |
Vii
Осн.
О
Сн2он
Снон Ч/�С»Н*
<;Н———- О
|
V |
|
СН30 |
![]()
|
Г VC-1TC’0H) ‘ |
I
Осн.
-о
VIII
Как видно из вышеприведенных формул, сформировавшийся лигнин содержит фурановые или пирановъш гетероциклы. В нем имеются два рода связей: кислородные простые эфирные мостики и наиболее проч ные связи через углерод. Подтверждением существования единого углеродного скелета у лигнина Фрейденберг считал стойкость последнего при нагревании с концентрированной йодистоводородной кислотой, расщепляющей лишь эфирные кислородные связи.
На основанжи предложенной схемы строения лигнина образование скелета вератровой кислоты можно представить следующим образом
—О—VcH-ctaw
N=<j-i—ц
Q
Как схематически показано, при сплавлении со щелочью расщепляются не только кислородные, но и углеродные связи. Подобным же образом можно представить и образование изогемипиновой кислоты, происходящее также с разрывом углеродной связи, но в другом месте.
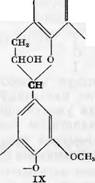
Свои выводы о механизме формирования лигнина из указанных мономерных единиц Фрейденберг основывал на сравнении с тщательно изученным медноаммиачным лигнином, получевным мягким методом. Анализ’ етого лигнина показал, что в нем содержится около 66°/0 С, 6.2°/0 Н, 16% ОСН3 и 9.5% О^Г. Примерно такому же составу соответствует продукт конденсации V. Фрейденберг охарактеризовал медно — аммиачный лигнин различными методами, о которых мы скаже м очень кратко.
|
Осн, |
|
Сн2 I I снон о |
|
СН2ОН СНОН |
|
СН |
|
I СII I 2 |
|
Осн3 |
30 Н. И Никитин
Наличие группы СН3—С(ОН)/ доказывалось им на основании оки
Сления медноаммиачного лигнина хромовой кислотой, при котором получалось до 6°/0 уксусной кислоты (вычислено 8.8°/0), наличие двойных связей бромированием не удалось определить. В процессе реакции бром становился в ароматическое ядро и выделялся бромистый водород по схеме
I I Вг
-f вг2 —> I ‘ + ИВг
|
/ |
|
ОСИ, |
|
О |
/Voch4
При этом на каждую мстоксильную группу в лигнин можно было ввести один прочно связанный атом брома. Небольшое количество двойных связей, как уже говорилось выше, было позднее обнаружено по реакции с тетраацетатом свинца
|
О I |
Ароматическая природа лигнина была подтверждена Фрейденбер — гом реакцией меркурирования [93]
^HgOCOCHg
-i — ch3cooii
+ Hg(OCOCII3)2 —
0
1
|
+ 2N02 |
С двуокисью азота медноаммиачный лигнин, как и все ароматические соединения, давал нитросоединение:
N0,
+ hno2
|
/ |
|
/уосн3 о |
|
Уосн3 о |
Для разъяснения химизма сплавления лигнина со щелочыо Фрей — денбергом было синтезировано более простое модельное вещество, так называемая кислота Эрдтмана, строение которой было доказано ранее. При сплавлении со щелочью в ней сперва происходило расщепление кислородного эфирного мостика по схеме
СООН COOK
I I
|
СН,—СН —! |
|
СН,—СН |
|
Осн. |
"V^OCH,
|
КОН |
|
СНОН ок I Уосн3 ОСНз |
|
СН—о I Уосн3 осн3 Кислота Эрдтмана |
После метилирования и окисления продукта сплавления были получены существенные количества вератровой и изогемипиновой кислот. Эта реакция объясняет процесс сплавления лигнина со щелочью, а также, по мнению Фрейденберга, служит указанием на механизм действия горячих щелочей на лигнин при щелочной варке.
Фрейденберг проводил сплавление со щелочью с последующим метилированием и окислением не только елового лигнина и еловой древесины, но также лигнина бука и буковой древесины. Как и следовало ожидать, из лиственного лигнина, кроме вератровой и изогемипиновой кислот, была получена в некотором количестве трпметилгалловая кислота
СООН
I
М
C! l3o/4/ocil3
ОСН3
Следует заметить, что если в лигнине присутствует сирингильная группа, т. е. если в нем содержатся и производные диметилпирогаллола, то ядерная конденсация, по-видимому, становится невозможной, так как оба орто-положения в ароматическом кольце по отношению к фенольному гидроксилу заняты метоксильными группами. Следовательно, можно ожидать, что лигнин лиственной древесины является менее конденсированным, чем лигнин хвойной древесины [®4].
Дальнейшее подтверждение своей теории Фрейденберг получил путем экспериментов по синтезу лигниноподобных продуктов при действии ферментов-дегидрогеназ, выделенных из сока гриба Psalliota Сат — Pestris, на конифериловый спирт.
СН=СН—СН2ОН I
I II
Конифериловый спирт
Были получены продукты, по химическим и физическим свойствам близкие к «нативному» еловому лигнину [96]. В подобных условиях си — наииновый спирт (сирингиловый аналог кониферилового спирта) дает продукт с содержанием метоксилов несколько более высоким, чем у нативного лигнина осины. Более подробно об этих исследованиях Фрей — денберга см. ниже, стр. 493.
|
Сп=сн—СН2ОН I 11 СНдО/у^ОСНз ОН Синапиновый спирт |
Из предшествующего весьма краткого и неполного очерка проведенных в 30-х и 40-х годах работ Фрейденберга видно, что этот автор тогда принимал существование единого углеродного скелета в древесном лигнине и, кроме того, наличие кислородных мостиков (простых эфирных связей). При дальнейшем обсуждении его работ другими химиками, выступившими со своим обширным экспериментальным материалом, представления Фрейденберга об едином углеродном скелете лигнина привлекли наибольшее внимание и встретили возражения. Самое крупное возражение заключалось в том, что 8—10-кратная поправка на выход изогемипи-
новой кислоты из лигнина ели, при сплавлении его и окислении, является чрезмерной, во много раз покрывающей найденную величину. Между тем именно на основании получения изогемипиновой кислоты при сплавлении, метилировании и окислении лигнина этот автор делал вывод о существовании единого углеродного скелета в лигнине.
Способ соединения всех мономерных частиц в лигнине при помощи только углеродных связей сейчас не считают единственно возможным. Отсутствие расщепления лигнина на мономеры при нагревании с крепкой йодистоводородной кислотой не является строго установленным, поскольку продукты этого расщепления (по кислородным мостикам) не летучи и их нельзя было уловить по методу Цейзеля. Поэтому не исключено, что мономерные фенилпропановые единицы лигнина могут соединяться друг с другом и без образования единого углеродного скелета, через кислородные эфирные связи, как предполагает на основании своих исследований Шорыгина (см. ниже, стр. 473).
В настоящее время Фрейденберг также пришел к выводу о наличии в лигнине не только углерод-углеродных связей в виде единого скелета, но и о соединении структурных единиц лигнина кислородными связями. Об этом более подробно будет сказано ниже, в других разделах (стр. 484 и 494).

 Опубликовано в рубрике
Опубликовано в рубрике