Важным критерием оценки активного угля-является распределение пор по радиусам или, иначе, распределение общего объема пор этого угля по их размерам. Расчет распределения пор обычно проводится по десорбционной ветви изотермы на основании так называемого уравнения Кельвина:
In pr = 2VMa cos ®/rRT (5.5)
Где р,— относительное давление; Ум— молярный объем; а — поверхностное натяжение адсорбта; О—угол смачивания (для азота близок к нулю); г — радиус пор; R— газовая постоянная; Т—абсолютная температура.
Это уравнение определяет тесную взаимосвязь между относительным давлением адсорбтива и радиусом пор, в которых при достижении этого давления газ конденсируется или вновь испаряется.
Простейший способ определения распределения пор состоит в постепенной десорбции использованного для измерений газа из насыщенного активного угля. Десорбируемое на каждой ступени (посредством снижения парциального давления) количество адсорбта соответствует в этом случае объему пор, опустошающихся на этой ступени десорбции. Однако при этом следует помнить, что в процессе десорбции поры освобождаются не полностью, в них остается адсорбированный слой, толщина которого зависит от парциального давления. Эту зависимость можно определить для непористых тел и рассчитать математически. Наиболее известные методы расчета разработали Крэнстон и Инкли [32], Пирс [33] и Липпенс, Линеен и де Бур [34].
|
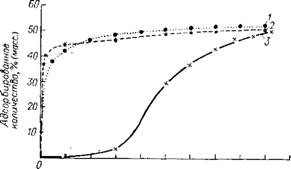
0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 Относительное давление Pr=P/Ps Рис. 5.12. Изотермы адсорбции: 1 — азот; 2 — пары бензола; 3 — пары воды. |
Обычно для адсорбционно-структуриого анализа используют изотерму адсорбции по азоту. Этот метод относительно трудоемкий и поэтому применяется только в некоторых специально оборудованных лабораториях. Определение распределения пор из изотермы обычно проводится по готовой вычислительной программе.
Измерения изотермы паров воды при комнатной температуре более просты и могут проводиться в каждой адсорбционной лаборатории. Однако установление равновесия водяного пара на активном угле происходит черезвычайно медленно, поэтому уже несколько десятков лет во многих лабораториях, особенно в Европе, в качестве адсорбтива используют пары бензола. Рачет изотермы бензола по 6—10 точкам измерения позволяет практикам достаточно точно охарактеризовать активный уголь, особенно в случаях, когда различные виды углей сравниваются по одному относительному параметру.
Для практической оценки адсорбционной способности активного угля обычно достаточно измерить 3—4 точки изотермы бензола. На рис. 5.12 приведены изотермы адсорбции азота, водяного пара и бензола на типичном газовом угле.
Де Бур [35] предложил новый метод анализа изотермы, основанный на расчете так называемого ^-распределения, т. е. толщины адсорбционной пленки (здесь T —■ относится к английскому «thickness»). Теория де Бура основана на представлениях о существовании адсорбционного равновесия между паром и поверхностью твердого тела. Если допустить, что покрытие, образующееся при определенном парциальном давлении, равномерно распределяется по поверхности твердого тела, тогда можно по объему адсорбта и поверхности БЭТ адсорбента рассчитать среднюю толщину покрытия. ^-Распределение получают из графика зависимости толщины адсорбционной пленки, возрастающей с повышением парциального давления, от
Парциального давления (или количества адсорбированного пара).
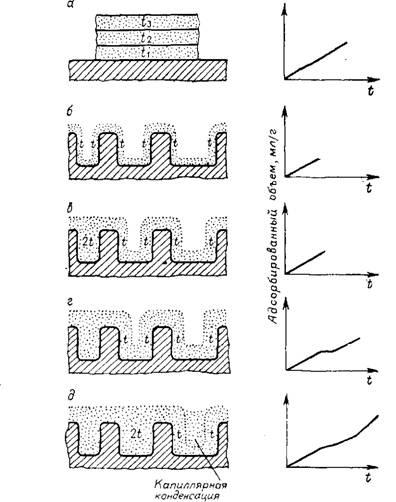
Для определения распределения пор можно использовать метод__сравнения ^-распределений для пористых тел с непористыми аналогами (рис. 5.13). На непористом твердом теле ^-распределение имеет вид прямой, наклон которой соответствует значению удельной поверхности (рис. 5.13, а).
Если метод де Бура используется для микропористых адсорбентов, например газовых или рекуперационных активных углей, то в начальной области относительных давлений зависимость количества адсорбированного вещества, удельной
|
*>ис’ 5 ‘3. Определение распределения пор по (-методу. |
|
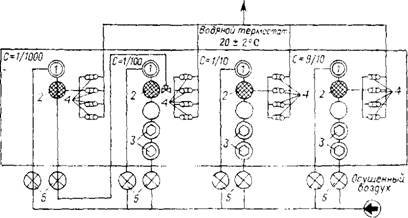
На сжигание
Рис. 5.14, Схема прибора для измерения изотермы адсорбции бензола: 1 — стеклянные спирали; 2— смесительные сосуды; 3 — промывные склянки с бензолом; 4—адсорбционные сосуды; 5 — расходомеры. |
Поверхности пор и толщины адсорбированного слоя T может быть представлена соотношениями:
Адсорбированный объем _ ,
—— г г————————- = 1олщина адсорбированного слоя T
Поверхность
Адсорбированный объем _
-7=——— £—£—:———————— г — Поверхность
Толщина адсорбированного слоя г
И /-распределение остается линейным (рис. 5.13, б).
С повышением парциального давления наступает момент, когда в результате слияния поверхностного покрытия противоположных стенок пор заполняются первые субмикропоры (рис. 5.13, в). Поверхность этих пор исключается из дальнейшего адсорбционного процесса, отмечается перегиб кривой насыщения, которая затем идет параллельно оси абсцисс. Это означает отсутствие пор в этом интервале линейных размеров. По соответствующему участку на ординате можно определить объем заполненных пор с диаметром 21.
В ходе дальнейших измерений кривая может снова отклониться вверх, хот’я наклон ее уменьшится в соответствии с имеющейся доступной поверхностью (рис. 5.13, г). Если с повышением парциального давления происходит капиллярная конденсация (рис. 5-13, д), появляется несоответствие между возрастающей адсорбционной емкостью и оставшейся поверхностью; на этом отрезке шкалы ^-кривая характеризуется крутым подъемом [35].
При постоянном парциальном давлении величина T связана ^ так называемым диаметром Кельвина D и истинным диаметром пор D следующим образом:
D — d + 2t (6.6)
|
Рг = Р! ро T, Нм Сi, нм D, нм Рг = plpo T, нм D, нм D, нм |
Ниже приведены значения этих величин для различных парциальных давлений паров бензола [36]:
|
0,001 |
0,01 |
0,03 0,06 |
0,10 |
0,18 |
0,3 |
|
0,024 |
0,166 |
0,284 0,344 |
0,38 |
0,42 |
0,47 |
|
0,61 |
0,92 |
1,19 1,49 |
1,82 |
2,45 |
3,49 |
|
0,64 |
1,25 |
1,77 2,18 |
2,58 |
3,29 |
4,43 |
|
0,4 |
0,6 |
0,7 |
0,8 |
0,85 |
0,9 |
|
0,52 |
0,72 |
0,87 |
1,06 |
1,2 |
1,44 |
|
4,58 |
8,32 |
11,8 |
18,8 |
25,8 |
39,9 |
|
5,62 |
9,66 |
13,5 |
20,9 |
28,2 |
42,8 |
В настоящее время наряду с азотом наиболее часто для определения изотерм адсорбции применяется бензол. Основной
|
?Н6. 5-15. Полуавтоматический прибор для измерения изотермы адсорбции бензола (фотография Лаборатории адсорбционной техники GmbH). |
Причиной его широкого использования является сравиителыи высокая стойкость бензола к разложению, исключающая ошиб ки измерения, вызываемые продуктами разложения; однакс токсичность бензола требует очень осторожной работы.
На практике опыт проводится в следующем порядке. Насыщенный парами бензола воздух смешивается в различных пропорциях с чистым воздухом, таким образом создается газовоздушный поток с относительными давлениями в пределах от 0,0001 до 0,95. В U-образных трубках или других соответствующих емкостях, помещенных в термостат, проводится насыщение образцов до постоянной массы, при этом опыт начинают с наибольшей концентрации, т, е. измеряется десорбционная ветвь петли гистерезиса.
На рис. 5.14 приведена схема классического аппарата с использованием в качестве адсорбтива бензола. В этом аппарате можно легко регулировать состав газовой смеси вручную; термостатирование осуществляется водяной ванной. Представленная на рис. 5.15 опытная аппаратура — полуавтоматическая: газовые потоки смешиваются автоматически; водяная баня заменена металлическим термостатом, поддерживающим постоянную температуру.

 Опубликовано в рубрике
Опубликовано в рубрике