Простейший фенол С6Н5ОН, резорцин С6Н4(ОН)21,3, о-, м- и п-кре — золы С6Н4СН3(ОН) способны извлекать лигнин из древесины (и переводить в раствор лигнин Вилыптеттера) при температуре около 90° в присутствии катализаторов, 0.03—1.0% соляной или серной кислоты. При этом происходит расщепление гидролизуемых химических связей между Лигнином и углеводами. Без катализатора фенол для извлечения лигнина требует нагревания до 180°. Лигнин с фенолом дает феноллигнин — химическое соединение, которое может быть высажено эфиром или получено в виде остатка от перегонки раствора с паром и очищено многократным высаживанием из ацетоно-эфирного раствора или из спирто-эфира. Феноллигнин представляет собой более или менее окрашенный аморфный порошок с начальной температурой плавления 190—195°. Феноллигнин растворим в ацетоне, метаноле, этаноле, пиридине, феноле и диоксане. Он может применяться в производстве пластмасс.
Существенный интерес имеет вопрос о характере связи между лигнином н фенолом. Был опубликован целый ряд работ и высказано несколько предположений относительно природы этой связи. Одно из предположений (Гильмер, [175]) основывается на возможности конденсации фенола с ароматическими структурными единицами лигнина с выделением воды. При этом одна молекула воды отщепляется за счет взаимодействия гидроксила лигнина и о-водорода фенола. Вторая молекула воды отщепляется вследствие реакции гидроксила фенола с водородом ароматических колец лигнина примерно по такой схеме
СН2ОН СН2ОН
|
СО I Си2 |
|
Со I Сн2 I |
|
<F____ >-оп + |
|
S V |
|
Учосн3 Он |
|
Уосн3 он |
Однако другие опыты показали, что в феноллигнине гидроксил фенола остается свободным. На это указывает хорошая растворимость феноллигнина в водном едком натре и некоторые другие факты. Эти данные наводят на мысль, что химическая связь между фенолом и лигнином осуществляется каким-то иным путем.
Одним из возможных способов реакции лигнина с фенолом моя<ет Быть конденсация карбонильной группы лигнина с водородом фенола, находящимся в орто- или пара-положении к группе ОН, например следующим образом
|
СН2ОН I Со I Сн2 I |
|
CHgOII -<f —сон |
|
Н0-<_>-Н + |
|
НО |
|
Сн2 I |
|
Учосн3 он |
|
YX°CH3 он |
Ушаков и Матвеев [75] пришли к заключению, что отщепление воды при образовании феноллигнина происходит не за счет гидроксильных групп лигнина или фенола, а вследствие вскрытия дополнительных гидроксилов в лигнине в процессе реакции.
Вачек [76], изучая реакцию фенолов с лигнином, получал различные феноллигнины: феноллигнин, n-крезоллигнин, п-хлорфеноллигнин и подвергал их окислению нитробензолом в щелочи. В качестве продуктов окисления были получены соответственно о-оксибензойная кислота I, 5,2-метилоксибензойная кислота II и 5,2-хлороксибензойная кислота III
СООН
TOC o "1-3" h z соон соон
|
I |
J ОН I /О II
Сн/4*/ СЛ^У
Ii iii
На основании этих результатов автор предположил, что фенолы конденсируются с лигнином с образованием углерод-углеродной связи в орто-положении но отношению к гидроксильной группе фенола.
Отметим еще, что недавно Чудаков |77 ] применил для исследования метод «термического растворения» фенол-лигнинового комплекса в среде жидкого растворителя (фенола) при высоких температурах (до 400°) и давлении. В качестве продукта реакции в значительном количестве им был получен дифениленоксид. Чудаков, разбирая возможный механизм реакции образования дифениленоксида, пришел к выводу, что фенол реагирует с боковой цепью фенилпропановой единицы лигнина.
Из противоречивых результатов многочисленных работ по изучению состава феноллигнина видно, что он является достаточно сложным. О строении этого продукта сейчас можно только с достаточной уверенностью сказать, что фенольные гидроксильные группы в основном остаются свободными при конденсации лигнина с фенолом.
В последнее время большое внимание уделяется возможной связи между фе- нолированием и сульфированием лигнина (см. главу «Сульфитная варка»). Так, например, Ишикава с сотрудниками [78| установил, что феноллигнин не сульфируется при сульфитной варке ни в нейтральной, ни в кислой среде. Если же лигнин предварительно метилирован диметилсульфатом, его фенолирование затрудняется. По мнению этих авторов, в реакции лигнина с фенолом важную роль играют те же свободные спиртовые гидроксилы, которые замещаются на сульфо — группы при сульфиронании лигнина
|
|
Как и при реакции сульфирования, скорость фенолпрования в большой мере зависит от рН. Часть реакционноспособных групп лигнина реагирует при высоких рН сравнительно быстро, другая часть медленно. Некоторые активные группы сульфируются и фенолируются лишь при рН, равном 1—2.5. Изучение ультрафиолетовых спектров поглощения феноллигнина и модельных соединений показало, что большая часть гидроксилов фенола и феноллигнине остается свободной.
Указанные японские авторы также нашли, что при действии фенола на лигно — сульфонаты происходит десульфирование и образуется феноллигнин. Оказалось, что часть сульфогрупп отщепляется легко, а часть более трудно, причем в низко — сульфированном лигнине содержатся только легко десульфирующиеся сульфо — группы, а в высокосульфированном и те и другие.
Точку зрения авторов о связи фенолирования и сульфирования подтверждают опыты, проведенные с модельными веществами: ванилиновым и вератровым спиртами.
|
CH2OII I /> |
|
СН2ОН I |
|
Уосн3 он Ванилиновый спирт |
|
, Ч0СН3 ОСН3 Вератровый спирт |
Фенолпроизводные этих спиртов не способны были сульфироваться ни в нейтральной, ни в кислой среде. При обработке же сульфопроизводных этих спиртов фенолом в присутствии 2—3% соляной кислоты при 60—70° С сульфопроизводное ванилинового спирта конденсировалось с фенолом количественно, а сульфопроизводное вератрового спирта — только на 20—30%.
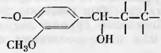
Реакпию фенола с модельными веществами, например с ванилиновым спиртом, можно представить следующим образом
|
>- |
|
Сн2-/ |
|
СИ2ОН I |
|
H- |
|
-ОН |
|
= |
Уон
|
УХ°снз ОН |
|
У�СНз он |
Полученное фенолпроизводное уже не может сульфироваться. Наоборот, сульфопроизводное ванилинового спирта может конденсироваться с фенолом по следующей схеме
|
Сн2 I |
|
=/ |
|
+ |
ОН СН,—Ч—Oil
CH2—SOsH н— I
H2S03 +
|
Уосн3 он |
|
Уосн3 он |

 Опубликовано в рубрике
Опубликовано в рубрике