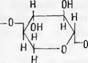
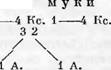Как уже указывалось, выделение пентозанов (как и всех гемицеллюлоз) из древесины обычно производится щелочью. Экспериментально было показано, что концентрация щелочи, равная 4°/0 весовым, является наилучшей для экстракции гемицеллюлоз (при 15°, 24 часа), так как при этом получается наибольший выход [2]. В табл. 124 приводятся данные, полученные в нашей лаборатории, которые иллюстрируют это положение.
Применение более крепкой щелочи для экстракции нежелательно, так как такая щелочь может оказывать влияние на другие составные части древесины, нять гемицеллюлозы.
При обработке щелочью опилок лиственных пород в раствор переходит главным образом ксилан с примесью небольших количеств другихгеми-
целлюлоз. Сырой ксилан может быть высажен нз раствора спиртом или ацетоном при подкислеции.
Для очистки сырого ксилана и получения более чистого препарата Сальковским [33] был предложен следующий способ. К щелочному раствору ксилана приливается фелингов раствор; при этом ксилан оседает в виде меднощелочного соединения. .Это соединение суспендируют в спирте и разлагают, пропуская газообразный НС] в спиртовую суспензию. Выделенный ксилан тщательно промывается и сушится.
Как показали наши опыты, режим такой обработки должен быть различным для кеиланов различных древесных пород. Ксилан, например, чозении требует более мягких условий очистки, чем ксилан дуба. Для того чтобы избегнуть разрушения полисахарида, целесообразно разлагать меднощелочные соединения 2 N раствором соляной кислоты.
За последние годы многие исследователи выделяли ксилан не непосредственно из растительного сырья, а из холоцеллюлозы [12, 13- 14 ], считая, что при такой обработке экстракция проходит полнее и легче. Однако последующие работы показали, что при делигнификации растительных материалов имеет место деградация цолисахаридов, и потому для выделения гемицеллюлоз предпочтительнее непосредственная экстракция щелочью [15]. Для предохранения полисахаридов от окисления во время обработки древесины щелочью целесообразно проводить экстракцию в атмосфере азота.
Ксилан представляет собой белый аморфный порошок без всякого запаха. Хорошо растворяется в щелочи; в воде сильно набухает. Нерас творим в спирте и органических растворителях. Не восстанавливает фелинговой жидкости. Щелочные растворы ксилана имеют сильное отрицательное вращение: различные авторы указывают для различных кеиланов величины от —78.2 до —109.5° L16].
Так же как и целлюлоза, ксилан относится к наиболее распространенным полисахаридам. В большем или меньшем количестве он находится во всех одревесневших растительных тканях: в древесине, соломе, мякине, лузге, хлопковой шелухе, в растении эспарто, в косточках слив, вишен и других плодов. Ксилан встречается во всех древесных породах, где он оказывается неизменным спутником целлюлозы.
В последнее время некоторые авторы высказывают предположение о существовании сложноэфирных связей между ксиланом и лигнином в древесине.
При гидролизе ксилана получается почти исключительно /)-ксилоза. Это в течение долгого времени давало основание считать, что ксилан построен только из ксилозы и представляет собой полимеризованный ангидрид ее. Однако многие авторы [2] находили в ксилане карбоксильные группы, метоксильные группы и остатки арабинозы. Решению вопроса о составе и структуре ксилана чрезвычайно мешало то обстоятельство, что исследователи не имели надежных методов выделения, очистки и разделения ксилана на фракции, а также достаточно точных методов исследования продуктов гидролиза полисахарида. Поэтому потребовался довольно длительный период, в течение которого были введены в технику химического анализа ионообменные смолы, хроматографический метод, мягкие методы метилирования и метанолиза полисахаридов, позволившие сделать в этом направлении большой шаг вперед.
Толчком, вызвавшим большой интерес к изучению гемицеллюлоз, в частности ксилана, и давшим целую серию работ в этой области, явилось сообщение Джонса и Уайза [17] о том, что ими найдена в гемицеллюлозах
В последующие годы различные исследователи нашли альдобиуроно — вую кислоту (идентичную с той, которая была найдена в древесине осины) также в древесине бука [16], березы [18], западного гемлока [1В]. 4-Метил — глюкозидуроноксилоза была найдена даже в целлюлозе, полученной из древесины березы, осины, сосны и ели [20]. Авторы считают, что эта кислота перешла в целлюлозу из древесины, где находилась в качестве составной части молекулы ксилана. Они отмечают, что содержание остатков уроновых кислот в целлюлозе придает ей свойство легко размалываться. Группы СООН увеличивают гидратацию целлюлозной массы, сильно набухают в воде и играют важную роль в образовании связей менаду волокнами в бумажном листе.
Дальнейшие исследования показали, что кислые компоненты гемицеллюлоз находятся в огромном большинстве растений в виде единиц 4-О—метил-/)-глюкуроновой кислоты,1 но связь их с молекулой ксилозы может осуществляться различно: через гидроксил при 3-м или 2-м углеродном атоме. Остатки уроновой кислоты обнаружены в гемицеллюлозах древесины сосны, ели, эвкалипта, различных североамериканских и финских древесных пород, в гемицеллюлозе кукурузной кочерыжки, соломы льна, пшеницы, овса, в древесных камедях и т. д.
В ксиланах соломы злаков и эспарто были найдены остатки L-арабо — фуранозы. В ксиланах соломы злаков находили также остатки /J-глюкуро- новой кислоты [13]. Изучение структуры ксиланов, выделенных из различных растительных материалов, показало, что здесь имеет место большое разнообразие в количестве и природе боковых цепей ксиланов при постоянной структуре главной цепи [5]. Основу всякого ксилана составляет цепь связанных в положении 1—4 остатков (3-£)-ксилопиранозы, имеющая различные ответвления.
Укажем, что обычным методом исследования структуры ксилана (как и всякого полисахарида) является метод исчерпывающего метилирования пентозана, последующего метанолиза (НС1 в метиловом спирте) и идентификации полученных продуктов. Наилучшие результаты получаются при мягком метилировании смесью йодистого метила с гидроокисью таллия, хотя возможно применение и других реагентов [21]. Если же необходимо провести гидролиз исходного материала, то для определения состава, например, древесного гидролизата и разделения полученной смеси углеводов с успехом могут быть применены ионообменные смолы. С их помощью кислые сахара отделяются от нейтральных. Для разделения же близких по свойствам веществ пользуются либо хромато — графической колонкой, либо методом бумажной хроматографии; последняя служит также целям идентификации. Идентификация может осуще —
|
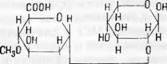
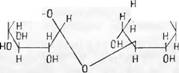
Осины 4-метил-0-глюкуроновая кислота, являющаяся составной частью альдобиуроновой кислоты, 2-а-(4-метил-/)-глюкуронозил)-1)-ксилозы, т. е. связанная с ксиланом |
|
Н |
|
Н ОН |
1 В этом соединении группа СН3 замещает атом водорода в гидроксиле 4-го углеродного атома глюкуроновой кислоты и таким образом связана с углеродом С4 через кислород. На это и указывает наименование «4-0-метил-£>-глюкуроновая кислота», которое иногда также пишется: «4-метил-£)-глюкуроновая кислота».
Ствляться различными путями. Часто пользуются реакцией восстановления при помощи гидрида лития, алюминия, а также реакцией окисления периодатом.
Таким образом, согласно современным исследованиям, все ксиланы наземных растений 1 содержат в качестве основы остатки p-D — кси л о п и р а — нозы, связанные в положении 1 —4, но различаются природой, количеством и характером связи других остатков Сахаров, присоединенных в виде боковых цепей. В боковых цепях могут встречаться остатки ксилозы, арабинозы или глюкуроновой кислоты. В том случае, если в молекуле ксилана присутствует уроновая кислота, образуемая ею с молекулой ксилозы, альдобиуроновая кислота может иметь не только структуру, указанную выше, но и другую, например
|
Поен И — —
|
В этом случае связь осуществляется через гидрокгил при С3 [6]. Ния<е приводятся структурные схемы ксиланов различного происхождения [•]. Обозначения приняты следующие: Кс. — р-D-ксилопи рано за; А.. — L-арабофураноза; К. г. — глюкуроновая кислота’
Ксилан клеточных стенок груши (плода)
Кс. 1—— 4 Кс. 1——- 4 Кс. 1——- 4 Кс. 1——- 4 Кс. 1——- 4 Кс. 1
3 3
Кс. 1——- 4 Кс. 1 I К. г.
Ксилан пшеничной
|
|
|
Кс. 1—— 4 Кс. 1——- 4 Кс. 1- 3 |
|
1 А. |
1 Только у ксилана водоросли Rhodymenia palmata найден несколько иной тип структуры [5]
Кс. 1——— 4 Кс 1——— 3 Кс. , — Кс.,
Гпе Кс. — остаток ксилозы. Зле»., связь осуществляете." не только между 1-м и 4-м углеродными атомами (Кс 1—4 Кс.), но и между 1 м и 3-м (Кс. 1—3 Кс). Длина цени этого ксилана 17 единиц.
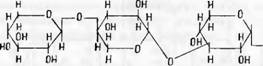
Для большей ясности напомним, что приводимые здесь структурные схемы являются общепринятым упрощением структурных формул. Схемы показывают, через какой атом углерода звена ксилозы осуществляется связь со следующим звеном. Вышеприведенный тип структуры, изображенный схематически, может быть изображен при помощи формул следующим образом
|
В дальнейшем мы будем пользоваться структурными ( хемами как болЯ простым способом изображения. |
Ксилан овсяной соломы
|
Кс. 1- |
|
-4 Кс. 1 2 |
|
-4 Кс. 1- |
|
-4 Кс. |
|
-4 Кс. 1- 3 |
|
1 А. |
1 К. г.
По данным Аспиналл и Мик [22], ксилан пшеничной соломы имеет структуру, выраженную следующей схемой (обозначения прежние)
-4 Кс. 1-
|
Кс. 1- |
|
-4 Кс. 1- |
|
-4 Кс. 1 |
2
|
Кс. 1- |
|
1 А. |
|
1 К. г. |
-4 Кс. 1
Исследования гемицеллюлоз европейского бука (Fagus Sylvatica), Проведенные Аспиналлом, Херстом и Махомедом [15], показали, что ксилан бука состоит из линейной цепи приблизительно 70 связанных в положении 1—4 (3-/?-ксилопиранозных единиц, из которых приблизительно каждая десятая несет 4-0-метил-/)-глюкуроновую кислоту. Последняя связана в качестве боковой цепи с ксилозой через углеродный атом С2. При исследовании гемицеллюлоз американского бука (Fagus Grandifolia) получены очень сходные с этими результаты. Молекула полисахарида здесь построена так же, как и в случае европейского бука, но составлена не из 70, а из 45 единиц ксилозы. Точка ответвления 4-0-метил-£»-глюкуроновой кислоты также находится при С2, но распределение единиц уроновой кислоты вдоль цепи ксилана неизвестно I28). Автор предполагает, что, может быть, на результаты изучения оказали влияние различные способы выделения гемицеллюлоз из древесины: для европейского бука применялась непосредственная экстракция древесины щелочью, для американского — экстракция холоцеллюлозы горячей водой.
Очень сходен с вышеописанным типом ксилана бука ксилан, выделенный из древесины обыкновенной ели [24]. Он составлен из 80—85 остатков |3-£>-ксилопиранозы, связанных в положении 1—4. Каждый пятый остаток (в среднем) несет концевой остаток 4-£)-метил-0-глюкуроновой кислоты, связанный с основной цепью через С2.
|
1-0-J |
|
Y-M Н он |
|
V |
|
Н он (^>Н,0Н |
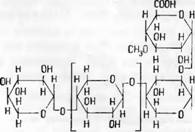
Из древесины березы (Betula Verrucosa) был выделен ксилан, построенный, примерно, из 22 ксилопиранозных единиц со связями 1—4. Главная цепь имеет точку ответвления в С2. Боковая цепь образована только одним остатком 4-0-метил-£)-глюкуроновой кислоты [1В]. Авторы приводят следующую структуру этого кислого ксилана
Этот ксилан также очень близок к описанному выше. В соответствии с этим авторы считают вероятным, что все твердые древесные породы содержат ксилан такого же типа. Для окончательного решения вопроса нужны дальнейшие исследования.
Работы Тимелла и сотрудников [25] показали, что гемицеллюлозы белой березы (Betula Papyrijera) содержат линейный полисахарид, состоящий из 110 (до 190) р-/)-ксилопиранозных остатков, соединенных связью 1—4. Со вторым углеродным атомом каждого одиннадцатого остатка ксилозы связан остаток 4-0-метил-/)-глюкуроновой кислоты. Очень сходную структуру имеют также полисахариды гемицеллюлоз ильма, желтой березы и сахарного клена.
Нужно указать также, что в ксилане, выделенном из холоцеллюлозы березы экстракцией диметилсульфоксидом [34], исследователи нашли 11.8% уроновых кислот и 16.9% ацетильных групп [36]. Последние связаны сложноэфирной связью [36] главным образом с третьим углеродным атомом звена ксилозы.
В ксилане европейской лиственницы, имеющем ту же структуру основной цепи, были найдены концевые остатки 4-6>-метил-/)—глюкуроновой кислоты и (в меньшем количестве) L-арабофуранозы, образующие боковые цепи. Точки ответвления находятся при С2 и С3 [2в].
В свете этих последних данных простое объяснение находит тот факт, что многие исследователи находили уроновые кислоты и метоксильные группы в ксилане ржаной соломы, дуба, клена и др. [2]. В лаборатории химии древесины Института леса АН СССР было найдено Цветаевой в ксилане дуба 8.5—10.9% уроновых кислот и 1.8—2.0% метоксильных групп, в ксилане чозении 11.3—11.5% уроновых кислот и 2.4—2.9% групп ОСН3. Очевидно, во всех этих случаях мы имеем дело с ксиланом, включающим в себя остатки этерифицпрованных уроновых кислот, подобно описанным выше.
Возможно, что приведенные выше новые данные о ксиланах позволят найти удовлетворительное объяснение различия свойств легко и трудно растворимого ксилана,[52] которое может быть обусловлено различным содержанием карбоксильных групп в различных фракциях вещества.
Гемицеллюлозы древесины могут содержать наряду с уже изученными также и другие типы ксиланов.
Суммируя изложенный выше материал, надо сказать, что в настоящее время исследованы многие древесные ксиланы и все они характеризуются присутствием (в качестве боковой цепи) остатков 4-0-метил-О-глюкуро — новой кислоты. Пропорциональное содержание уроновой кислоты в общем несколько выше в ксиланах мягких, т. е. хвойных пород (гемлок, ель, лиственница), где оно составляет 15—20%, чем в ксиланах твердых (лиственных) пород (бук, береза, осина), где оно колеблется в пределах 8—15% [26]. Некоторые древесные ксиланы содержат также небольшие количества jL-арабофуранозьт. Наоборот, ксиланы злаков характеризуются в общем более высоким содержанием арабинозы и более низким содержанием уроновых кислот. Все изученные древесные ксиланы оказались линейными полимерами, содержащими только единичные боковые цепи, тогда как ксиланы не древесных растений (экспарто, кукуруза, солома) содержат разветвленную цепь молекул.
Хотя последние данные позволили во многом уточнить структуру различных ксиланов, тем не менее отдельные вопросы остались еще неясными и пока еще невозможно четко разграничить детали структуры ксилапов различных растительных тканей.
Проблема природы, распределения и относительного количества боковых цепей в ксиланах важна потому, что эти группы определяют в большой мере свойства этих полисахаридов и, следовательно, также их поведение в технологических процессах. Все эти вопросы должны окончательно разъясниться в ходе дальнейших исследований.
Что касается величины и формы молекулы ксилана, то, основываясь на приведенном выше материале, можно считать, что величина молекулы может быть различной. В одном из более ранних исследований СП ксилана бука была найдена равной 150 I27]. Выше нами были указаны величины СП ксилана от 22 до 80. Различные авторы находили различные величины СП этого полисахарида: от 35 [2] до 185 [13]. Очевидно, возможны широкие колебания в размерах молекул.
Здесь надо указать, что полученные некоторыми авторами кристаллические ксиланы [13′ 14] имеют меньшую СП, чем ксиланы исходных гемицеллюлоз. При получении кристаллических ксиланов ячменя, пшеницы, ржи Бишоп [13] отметил значительную деградацию молекулы, приведшую к уменьшению молекулы до [53]/3—1/е первоначальной длины.
Форма молекулы ксилана, по-видимому, более постоянна и имеет це — певидный характер. Разветвления в цепи редкие, и боковые цепи короткие. Такие представления совпадают с данными более ранних исследований ксилана бука, приведенными в работе Хуземан I27].
В этой же работе [27] автор изучала ксилан бука с точки зрения молекулярной однородности и пришла к выводу, что около 95% ксилана состоит из цепей одинаковой длины. Ксилан как будто бы не является полимолекулярным веществом.
Ксилан обладает двумя свободными гидроксилами в каждом остатке ксилозы и поэтому способен давать простые и сложные эфиры. Различными авторами (Солечник, Конкин, Роговин и др.) [21] были получены метил — и бензил-ксиланы, а также нитроксилан и ацетилксилан. Изучались и другие эфиры ксилана.
Ксилан имеет практическое значение в народном хозяйстве и может быть использован как сам по себе, так и в виде ксилозы, которая является главной составляющей и главным продуктом гидролиза этого полисахарида. Неоднократно отмечался исследователями тот факт, что присутствие ксилана (как и других гемицеллюлоз) в клеточных стенках увеличивает набухание последних и содействует размолу и гидратации целлюлозной массы в роллах, что в свою очередь способствует образованию прочного бумажного листа.1
При действии 10%-й йодной кислоты на ксилан окисляются гидро — ксильные группы у второго и третьего углеродных атомов (гликолевая группировка) с образованием диальдегидксилана, который при дальнейшем гидролизе разбавленной минеральной кислотой дает глицериновый альдегид и глиоксаль
СНгОН-СНОН-С^° глицериновый альЗегиЭ
|
О о II II С-Н Н-С н |
|
|
|
НЭОл |
|
Y N — «т—Л*— |
|
ГиЗролиз |
H/L ХН Глиоксаль
Из глицеринового альдегида получают метилглиоксалъ или глицериновую кислоту. Глицериновую кислоту СН2ОН—СНОН—СООН наряду. с глиоксалевой СНО—СООН можно также получить при окислении и последующем гидролизе диальдегидксилана.
При гидрировании диальдегидксилана в определенных условиях получается полимерный алкоголь. Этот последний, будучи подвергнут гидролизу, а затем гидрированию, дает смесь глицерина и гликоля по следующей схеме
|
ОН он |
|
-о — Богстсн. -0- |
|
/ |
|
Н*с |
|
Н/С-н н-С |
|
Снг н |
Сн2он-снон-снгон глицерин
ГиЗролиз
И6осстан. _ н
Продукт гидролиза ксилана — ксилоза — является весьма ценным веществом. Она может быть использована в качестве кормов, применяется в медицинской и фармацевтической промышленности, а также как сырье для получения триоксиглутаровой кислоты, фурфурола, кормовых дрожжей и т. д.
Источником ксилозы может быть не только древесина, но и отходы сельского хозяйства (солома, мякина, лузга, кукурузные початки, хлопковая шелуха и т. д.), содержащие до 35% пентозанов (ксилана).
При окислении ксилозы азотной кислотой получается триоксиглута — ровая кислота, которая может заменить лимонную кислоту в кондитерском производстве и в медицине (стабилизация крови).
C<f СООН СООН
IХН | |
Н_с—ОН Н—С—ОН Н—С—он
Окисление | окисление
II—С—ОН Н—с—ОН II—С—ОН
I I I
СН2ОН СН2ОН соон
Ксилоза Нейлоновая Триоксиглутаровая
Кислота кислота
Процесс получения триоксиглутаровой кислоты детально разработан Чаловым[28].
При гидрировании ксилозы получается пятиатомный спирт—-ксилит, который используется как заменитель глицерина 27 Н. И. Никитин
|
|
|
Н—С—он |
СН2ОН
Н—С—ои
|
|
|
Но—с—н Н—С—он |
СН2ОН
На основе ксилита получен новый вид искусственных смол — кси — фтали. Они образуются при полимеризации эфиров, получающихся при этерификации ксилита фталевым ангидридом в определенных условиях.
Хорошо изучен азотнокислый эфир (пентанитрат) ксилита. В последнее время получены Аникеевой и Зарубинским [29] аллиловый и метал — лиловый эфиры ацеталей и кеталей ксилита.
Ксилоза (как и все пентозы) не способна сбраживаться дрожжами на спирт, но она вполне пригодна для выращивания кормовых дрожжей. На пентозных гидролизатах растут дрожжи Monilia Murmanica, Torula La, Torula E.L() и др. Пентозы сульфитных щелоков могут быть использованы как источник углеводного питания для дрожжей, образующих жиры (близкие к растительным) и белки.
Некоторые бактерии и грибки могут сбраживать ксилозу с образованием ацетона, бутанола (ацетоно-бутиловые бактерии), лимонной (Aspergillus Niger Citromyces), уксусной и молочной кислоты (Bacillus Pentosus).

 Опубликовано в рубрике
Опубликовано в рубрике