3.1. ТЕРМИНЫ И ОПРЕДЕЛЕНИЯ
Концентрирование вещества на поверхности раздела фаз принято называть сорбцией. Если концентрирование происходит только на поверхности, процесс называется адсорбцией. Адсорбция на твердых телах может протекать из газовых фаз и жидких сред. При этом необходимо различать физическую адсорбцию и хемосорбцию (см. ниже). Если сорбируемые молекулы проникают в объем соседней фазы, мы говорим об абсорбции, например, при наводороживании некоторых металлов или растворении газов в жидкостях. Под десорбцией следует понимать процесс, обратный адсорбции.
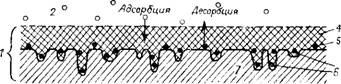
В соответствии с постановлением IUPAC от 1972 г. адсорбирующее средство принято называть адсорбентом, а адсорбируемое вещество — адсорбтивом. В адсорбированном состоянии оно называется адсорбтом. Под адсорбатом подразумевается система адсорбент + адсорбт в целом (рис. 3.1).
3.2. ФИЗИЧЕСКАЯ АДСОРБЦИЯ. ХЕМОСОРБЦИЯ
Физическая адсорбция обусловлена в основном ван-дер-ва- альсовыми силами. В этом процессе адсорбированное соединение не подвергается химическому изменению. Наряду с этим известен также процесс, обычно называемый хемосорбцией. Такой тип сорбциониого процесса, подобно другим химическим превращениям, отличается большой энергией активации; при этом возникает химическая связь, изменяющая химическую природу сорбированной молекулы. В большинстве случаев при хемосорбции возникают более прочные связи, чем при физической адсорбции, хотя иногда возможно промежуточное явление— так называемая легко обратимая хемосорбция. Наряду с такими теоретическими различиями оба процесса имеют следующие характерные практические различия.
1. Физическая адсорбция вещества в значительной степени протекает в области температур, близких к точке кипения или несколько выше; хемосорбция происходит при температурах, значительно превышающих температуру кипения.
2. Хемосорбция, требующая высокой энергии активации, зависит от температуры: чтобы процесс протекал с достаточной скоростью, необходима определенная минимальная температура. Физическая адсорбция, напротив, эффективнее протекает при низких температурах.
3. Хемосорбция — процесс специфический в основном для соединений, способных вступать в реакцию с твердым телом; физическая адсорбция, напротив, относительно неспецифична.
4. При физической адсорбции наблюдается положительный тепловой эффект, приближенно равный теплоте конденсации (т. е. нескольким кДж/моль). Теплота реакции в процессах хемосорбции заметно выше и составляет обычно 10— 60 кДж/моль.
5. При физической адсорбции на поверхности адсорбента может образоваться несколько адсорбционных слоев (см. раздел 3.4). Хемосорбция протекает только с образованием монослоя; в этом случае массообмен незначителен.
3.3. ТЕОРЕТИЧЕСКИЕ ОСНОВЫ. ПОТЕНЦИАЛЬНАЯ ТЕОРИЯ
Описание адсорбционных процессов, соответствующее современным научным представлениям, в основном сформулировано Поляни [1] как теория адсорбционного потенциала, а позднее развито Дубининым и сотрудниками [2, 3]. Уравнение Дубинина — Радушкевича (см. ниже) придало этой теории практическое значение.
Основное допущение потенциальной теории состоит в том, что на поверхности твердого тела действуют силы притяжения, в частности, так называемые дисперсионные силы, которые создают силовое поле (потенциальное поле). Эти силы, а следовательно, и потенциальное поле, действуют на коротких расстояниях. Действие различных сил ослабляется обратно пропорционально расстоянию в некоторой степени. Значение показателя степени приводится в табл. 3.1.
|
О—— 3 |
|
Рис. 3.1. Схема процесса адсорбции: I — адсорбат; 2 — газовая или жидкая фаза; 3 — адсорбтив; 4 — поверхностная пленка; 5—адсорбт; 6 — активные центры; 7 — адсорбент. |
Область действия сил притяжения характеризуется так называемым адсорбционным потенциалом, который представляет собой работу, выполняемую силами адсорбции при переносе
частицы из окружающего газового пространства на поверхность или близко к ней. Этот термодинамический потенциал является наибольшим на поверхности твердого тела и с увеличением расстояния от поверхности быстро уменьшается. Адсорбция также возможна только в непосредственной близости к поверхности. Для однородной поверхности все точки, равноотстоящие от поверхности твердого тела, имеют одинаковый потенциал и расположены в одной эквипотенциальной плоскости. Каждая" такая эквипотенциальная плоскость ограничивает определенный объем Wx и характеризуется собственным потенциалом Ех. Максимальный объем Wo ограничен потенциальной плоскостью с потенциалом, равным нулю, только в этом объеме возможна адсорбция (рис. 3.2).
Поляни определил адсорбционный потенциал Е как работу изотермического сжатия, которую необходимо выполнить, чтобы довести пар с равновесным давлением р до давления пара сжатого адсорбта рц на данной эквипотенциальной поверхности:
TOC o "1-3" h z Е — RT in (Р2/Р1) (3.1)
Где R — газовая постоянная; Т—абсолютная температура.
|
ТАБЛИЦА 3.1. Силы адсорбционного взаимодействия [4]
Физическая адсорбция Кулоповское притяжение между заряженными частицами Силы притяжения между двумя диполями Силы притяжения между ионом и диполем Силы взаимодействия между нейтральными частицами (дисперсионные силы) Обменные силы (гомеополярная химическая связь) |
|
Mr2 Mr7 I/г* Mr7 L/r’o — l/r13 |
|
Хемосорбция |
А 6
|
|
………………………………….. F„«0 ………… ………………………… £п=0
Е2
|
Vhc. 3.2. Эквипотенциальная поверхность Поляни: а — однородная поверхность; б — неоднородная поверхность. |
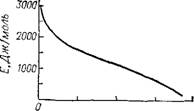
Рис. 3.3. Характеристическая кривая адсорбции паров бензола на активном угле.
При температурах ниже критической температуры пара потенциал Е представляет собой работу сжатия от равновесного давления р до давления насыщенных паров жидкости Ps при температуре окружающей среды:
E^RTln (ps/p) (3.2)
|
0,1 0,2 О,J АУ„,см*/г |
Если допустить, что адсорбция представляет собой переход газа в жидкое состояние, плотность адсорбированных паров можно выразить через плотность вещества в жидком состоянии при соответствующей температуре. Соответственно заполненный объем пор W можно вычислить из следующей зависимости:
|
|
|
(3.3) |
|
W |
С/рг = аМ/рт = AV F
Где G — масса адсорбированного пара; рг — плотность соответствующей жидкости при температуре Т а — адсорбированное количество вещества, моль; М — молекулярная масса; Ум — мольный объем жидкости при температуре Т.
Решающий толчок развитию потенциальной теории дали работы Дубинина и Радушкевича; определяя значения адсорбционного потенциала отдельных веществ в зависимости от степени заполнения адсорбционного пространства [уравнение (3.3)], они получили гауссовское распределение так называемых характеристических кривых (рис. 3.3) и вывели уравнение, описывающее эти кривые:
W = W0e’№ (3.4)
Где K — константа.
Авторы рассматривали эти характеристические кривые как статистические кривые, которые описывают объем W как часть объема адсорбционного пространства W0, заполняющуюся ад — сорбтом при потенциале Е.
Подставив уравнения (3.2) и (3.3) в выражение (3.4) и решая его для а, получаем:
(3.5)
Постоянную величину KR2 можно заменить:
TOC o "1-3" h z kRZ = В/р2 (3.6)
Где В — новая константа; р — так называемый коэффициент аффинности.
После преобразования
« = (3.7)
Получаем обычное уравнение Дубинина — Радушкевича в логарифмической форме:
Lg А = lg (WJVM) — 0,434В (Р/р») [lg (ps/p)Ja (3.8)
где а — количество адсорбта, ммоль; 1F0 — предельный объем адсорбционного пространства (рассчитывается из характеристической кривой); Vm— объем 1 ммоль вещества, в адсорбированном состоянии, см3; В — константа, которая рассчитывается подстановкой в уравнение (3.8) известных величин изотермы; Ps — давление насыщенных паров адсорбта при Т; р — парциальное давление адсорбтива в газовой фазе при Т.
Уравнение (3.8) содержит два члена, из которых lg(W0/VM) выражает состояние максимальной адсорбции, а вычитаемый член включает параметры, обусловливающие снижение адсорбции. С помощью уравнения Дубинина по изотерме, измеренной для определенной системы адсорбент — адсорбтив, можно рассчитать ход кривых для всех других температур. Кроме того, зная мольный объем давление паров и коэффициенты аффинности других паров, можно рассчитать изотермы адсорбции этих паров на данном угле. Значение безразмерного коэффициента аффинности |3 в первом приближении не зависит от температуры. Его можно взять для многих паров из литературных источников [5, 6], причем в качестве стандартного адсорбтива обычно выбирают бензол:
|
Р |
Р |
||
|
Бензол |
1,00 |
Бутан |
0,90 |
|
Метанол |
0,40 |
Циклогексан |
1,04 |
|
Этанол |
0,61 |
Пентан |
1,12 |
|
Дихлорметан |
0,66 |
Толуол |
1,25 |
|
Хлорэтан |
0,76 |
Хлорпикрин |
1,28 |
|
Пропан |
0,78 |
Гексан |
1,35 |
|
Хлороформ |
0,86 |
Гептан |
1,59 |
|
Ацетон |
0,88 |
Следует отметить, что уравнение (3.8) в приведенной форме можно применять только для адсорбентов / структурного типа (см. раздел 3.5.1), к которому, однако, относится большинство газоадсорбционных углей. Для адсорбентов II структурного типа, а также при температурах выше критической необходимы поправки или соответствующие модификации уравнения, усложняющие его применение. Следует также заметить, что уравнение Дубинина — Радушкевича справедливо только для парциальных давлений ниже давлений капиллярной конденсации (см. раздел 3.4).
Несмотря на весьма привлекательные возможности уравнение (3.8) до сих пор не получило широкого распространения, поскольку на практике приходится иметь дело почти исключительно с адсорбцией смесей.
3.4. КАПИЛЛЯРНАЯ КОНДЕНСАЦИЯ
Если проследить за увеличением сорбционной емкости активного угля по отношению к пару с ростом парциального давления пара до насыщения, то в области относительного насыщения выше 30 % можно наблюдать сильное увеличение поглощения паров. Напротив, при постепенной десорбции с пони-
|
Ряс. 3.4. Петля гистерезиса: десорбция; адсорбция. |
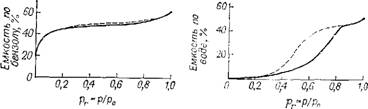
Жением парциального давления получаем десорбционную ветвь, которая в определенной области характеризуется более высоким поглощением, чем адсорбционная ветвь. Такое явление называется гистерезисом (рис. 3.4).
Явление гистерезиса можно объяснить, с одной стороны, пористой структурой активных углей, а с другой — поведением конденсированного пара. При низких парциальных давлениях поверхность угля покрывается адсорбированным слоем прежде всего в местах с наиболее высокой плотностью энергии и с повышением парциального давления образуется мономолекулярное покрытие (в статическом смысле). Фактически еще до завершения полного покрытия на поверхности угля происходит локализованная полимолекулярная адсорбция — появляются плоские «лужицы». В узких порах с диаметром порядка четырех диаметров молекулы пара с увеличением толщины слоя адсорбта образуется жидкий мениск. Поскольку все органические жидкости смачивают активный уголь, образуется вогнутый жидкий мениск. Действующие на поверхности этого мениска силы стягивания приводят к снижению давления паров по сравнению с плоской поверхностью. Поэтому капиллярная конденсация происходит в порах еще до того, как будет достигнуто давление насыщения вне пористой системы. По тем же причинам во второй части описанного выше эксперимента снижение давления паров сопровождается замедленной десорбцией и появлением вышеупомянутого гистерезиса. Для описания гистерезиса наряду с другими моделями часто используется так называемая теория бутылкообразных пор [7]. Согласно этой теории сорбенты, характеризующиеся гистерезисными петлями, содержат поры с узкими входами. Конденсация при адсорбции происходит в порах с наибольшим диаметром — в полости «бутылок». Десорбция лимитируется диаметром узких горл бутылок; таким образом процесс десорбции, соответствующий адсорбции, возможен только при более низком парциальном давлении. По виду и ширине петли гистерезиса можно сделать заключение о форме пор [8, 9].
Количественная зависимость между снижением давления в сорбирующих порах и их диаметром впервые сформулирована Кельвином [10]:
RT In (р/р,) = 2а cos WM/r (3.9)
Рие. 3.5. Зависимость изотермы адсорбции паров воды от угля смачивания (гидрофобности) угля:
|
К |
|
1С20 «э Ч |
I — окисленный уголь; 2 — необработанный уголь; 3 — прокаленный уголь.
Где р — давление пара в капилляре; Ps — Давление насыщенного пара при температуре опыта; а — поверхностное натяжение чистой жидкости; VM — мольный объем жидкости; О — угол смачивания поверхности угля исследуемой жидкостью.
Решая это уравнение для г, можно рассчитать распределение пор по размерам, используя изотерму адсорбции или десорбции любого пара, например азота, воды или бензола при температуре, близкой к точке кипения [11]:
Г = 2О cos bVMjRT In (p/p,) (3.10)
Во многих случаях возникают трудности при определении угла смачивания О, который для различных паров зависит от вида и количества кислородных соединений на поверхности угля. Влияние угла на изотерму адсорбции паров воды показано на рис. 3.5, при этом изотерма измерялась на свежепро — каленном, необработанном и покрытом поверхностными оксидами активном угле.

 Опубликовано в рубрике
Опубликовано в рубрике