Нитроцеллюлоза не устойчива к действию кислот и щелочей. При действии на нитроцеллюлозу разбавленных минеральных кислот происходит медленная денитрация при одновременном гидролитическом разрушении цепей.
Концентрированная серная кислота растворяет нитроцеллюлозу на холоду. При этом количественно выделяется азотная кислота.
Щелочи действуют на нитроцеллюлозу энергично — омыляя и разрушая ее.
Разбавленные водные растворы щелочи на холоду действуют на нитроцеллюлозу, медленно, так как последняя плохо смачивается ими. Спиртовые растворы щелочи той же концентрации быстро омыляют и деструк- тируют нитроцеллюлозу. В результате обработки щелочью получаются продукты, свидетельствующие о глубокой деградации целлюлозы: углекислый газ, муравьиная, масляная и пировиноградная кислоты, редуцирующие вещества и азотсодержащие продукты [28].
Вследствие этого при денитрации щелочью нельзя получить неизменную или малоизмененную целлюлозу. Регенерацию целлюлозы из ее нитрата можно провести в мягких условиях, используя другие омыляю — щие реагенты, например кислые соли сероводородной кислоты — гидросульфиды натрия и аммония.
Реакция происходит по следующей схеме
[C6H7020H(0]N02)2]„ h2’lNaSH —> [С6Н702(0Н)3]и + 2nNaN02 Ь2«S
Однако при регенерации целлюлозы даже в мягких условиях, к; было показано Роговиным [29], происходит значительная деструкция целлюлозы.
Нитроцеллюлозы являются неустойчивыми, особенно в сухом состоянии, к действию тепла соединениями. Стойкость их проверяется различными методами, например пробой Бергмана и Юнка [8, стр. 273].
Температура воспламенения зависит от скорости подвода тепла: при достаточно медленном нагревании она порядке 1У0°, при быстром нагревании — 160—170° I4, стр. 110].
Термическое разложение нитроцеллюлозы сопровождается выделением большого количества газов. В соответствии с полученными ранее результатами Андреев и Самсонов [31] недавно показали, что при термическом распаде нитроклетчатки в замкнутом объеме газообразование идет со значительным ускорением. При этом газов образуется значительно больше, чем при разложении в вакууме, а вес остающегося твердого остатка оказывается меньше.
Опыты этих авторов по разложению нитроклетчатки в вакууме показали, что такое влияние газообразных продуктов распада объясняется главным образом взаимодействием их реакционноспособных компонентов друг с другом и с твердыми веществом, ведущим к образованию’ дополнительных объемов газа.
Среди газообразных продуктов реакций термического распада нитроцеллюлозы обнаруживают, кроме различных окислов азота, углеродсо — держащие летучие вещества и газы — С02, СО, муравьиную кислоту,, формальдегид, глиоксаль и HCN.
Исследования термического распада, проведенные на радиоактивном нитрате целлюлозы (С14), показали [32], что, вероятно, глиоксаль образуется из углеродного атома во 2-м положении (С2) и примыкающих углеродных атомов, а двуокисьн углерода и муравьиная кислота в основном из ЈJ а также из С2 и СБ.
Основное количество формальдегида образуется из 6-го углеродного» атома.
|
Н 0N0Z |
|
НС=0 |
|
Сульфоэфиры целлюлозы Концентрированная серная кислота (от 72% и выше)- быстро растворяет целлюлозу на холоду, образуя прозрачные растворы. При стоянии растворов происходит их почернение в результате обугливания целлюлозы. К такому же эффекту приводит повышение температуры. |
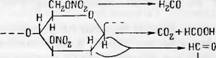
Таким образом, принципиальная начальная схема термического разложения нитроцеллюлозы такова
Высаженная из раствора серной кислоты сразу же после растворения в ней целлюлоза гидролизована и почти не содержит связанной серы. Однако при более длительном контакте целлюлозы с серной кислотой, как было показано еще Браконно и Кароллесом I33], увеличивается количество Ба, связанного с целлюлозой в результате обмена.
При стоянии раствора целлюлозы в H2S04 в течение 24 часов при комнатной температуре образуется, по данным Кароллеса, Ва-соль сульфо — чфира целлюлозы, имеющая состав C4II804(S03)2Ba0 -2Н20 с соотношением Ва к H2S04 в соли 1 : 2.
Траубе, Блазер и Грюнерт [34] получили трисульфат целлюлозы при действии на сухую целлюлозу паров S03. Калиевая соль этого эфира целлюлозы, полученная с 65%-м выходом, имела ссстав СвН702(Ь03К)3.
В качестве другого метода получения сернокислых эфиров целлюлозы использовали также этерификацию целлюлозы хлорсульфоновой кислотой (CIS03H) в присутствии пиридина.
Анализ полученных продуктов показал, что они имели степень замещения, близкую к 3.
В многочисленных патентах, предложенных затем для получения этого яфира целлюлозы, указывалось на возможность этерификации целлюлозы S03 в присутствии пиридина или четвертичных аммониевых оснований, пиросерной кислотой (H2S207) в присутствии органических основании, этерификации в присутствии NaOH и т. п. I35].
Однако этерификации целлюлозы серной кислотой в гомогенных условиях или другими реагентами относительно сложна и не применялась еще сравнительно недавно в промышленности.
Вместе с тем эфиры целлюлозы и серной кислоты представляют интерес, так как они растворимы в воде и, следовательно, могут быть использованы, как и другие водо — и щелочерастворимые эфиры.
В последнее время были разработаны способы получения сульфо — эфиров в гетерогенной среде, значительно упрощающие проведение этой реакции, благодаря чему сульфоэфиры целлюлозы получили промышленное значение.
К указанным способам этерификации относится главным образом этерификация в гетерогенных условиях бинарными смесями серной кислоты и алифатического спирта.
Так, например, в одном из патентов [361 предварительно активированная целлюлоза погружалась в 40%-й раствор 95%-ой H2S04 в ледяной уксусной кислоте при 3°. Избыток жидкости отфильтровывался, целлюлоза отжималась и после размельчения диспергировалась при перемешивании в метиленхлориде.
Суспензия в метиленхлориде перемешивалась при +3° в течение 1.75 час. К концу этого периода избыток жидкости декантировался и сульфат целлюлозы промыьался сначала охлажденным до —10° изопро — пиловым спиртом, а затем водой. Полученный таким образом продукт сохранял волокнистую структуру, содержал 4.5% серы, что соответствует степени замещения у = 27. Сульфат целлюлозы полностью растворялся в воде.
Роговин и Мирлас [37] проводили сульфатирование целлюлозы смесью, содержащей 80% H2S04 (концентрация — 95—96%) и 20% изобутило — вого спирта.
Хлопковая целлюлоза обрабатывалась этой смесью при 5—7° и модуле ванны 14. После окончания реакции, которая длилась 1.5 час., продукт
реакции, сохранивший волокнистую структуру, отжимался от избытка этерифицирующей смеси и промывался изобутиловым спиртом.
Остатки кислоты нейтрализовались спиртовым раствором КОН, поели чего продукт вновь промывался спиртом. Такой способ этерификации
|
Таблица 84 Гидролиз пиридиновой соли три сульфоэфира целлюлозы (460/0 H2S04)
|
Позволяет получить препараты сульфо-1 эфира целлюлозы с невысокой ст~ пенью этерификации (у~50), полностью растворимые в воде с образованием вязких растворов.

 Опубликовано в рубрике
Опубликовано в рубрике