Характеристика гидролизатов и сульфитных щелоков как питательной среды
Гидролизаты, получаемые в результате гидролиза древесных и сельскохозяйственных отходов, а также сульфитные щелока являются средой, неблагоприятной и недостаточно полноценной
Для жизнедеятельности микроорганизмов. Наиболее ценными веществами гидролизатов и сульфитных щелоков являются моносахариды, состоящие из гексоз с общей формулой С6Н120б, и пен — тоз, имеющих формулу С5Н10О5.
В гидролизатах, полученных при гидролизе разбавленными кислотами, содержится в среднем 2,0—3,1% гексоз и 0,6—1,0% пентоз. Сбраживаемыми на спирт сахарами являются гексозы, в состав которых входит глюкоза, манноза, галактоза и иногда фруктоза. Труднее других Сахаров сбраживается галактоза. В состав несбраживаемых на спирт пентоз входят ксилоза и араби — ноза. В небольшом количестве в гидролизатах встречаются метилпентозы, а также частично гидролизованные полисахариды (декстрины). Наряду с сахарами в гидролизатах содержится ряд веществ, отрицательно влияющих на жизнедеятельность микроорганизмов. К ним относятся: а) серная кислота (0,5—0,8%), являющаяся катализатором при гидролизе; б) органические — уксусная, муравьиная, левулиновая, пропионовая, уроновые, смоляные и высшие жирные кислоты (0,3—0,4%). Благодаря наличию этих кислот активная кислотность гидролизата колеблется в пределах рН=1,0—2,5; в) продукты разложения Сахаров и побочные продукты гидролиза: фурфурол (0,03—0,06%); оксиме — тилфурфурол (0,12—0,16%), метиловый спирт (0,02—0,03%); формальдегид, ацетон, терпены (0,05—0,06%); г) коллоидные вещества — лигниновые и гуминовые; находясь в гидролизатах в виде тонкодисперсных коллоидных веществ, они могут адсорбироваться на поверхности дрожжевой клетки, уменьшая ее активную поверхность и тормозя процесс ее обмена. В состав гидролизатов входят также минеральные вещества. Все эти вещества находятся в водном растворе.
Гидролизаты, полученные в результате гидролиза лиственной древесины и сельскохозяйственных отходов, имеют несколько иной состав. В них содержится больше пентоз (4—6%), фурфурола (0,1—0,2%), уроновых кислот и меньше гексоз, а также нет терпенов. Сельскохозяйственные гидролизаты содержат больше минеральных и азотистых веществ.
Температура гидролизатов после испарителей колеблется в пределах 90—98°.
В отличие от растительных гидролизатов сульфитный щелок имеет более сложный состав. В нем содержится меньше, чем в гидролизате, моносахаридов (1,8—3,1 %’, в зависимости от жесткости сульфитной варки). Из них гексозы составляют 1,1—2,2%. а пентозы 0,7—0,9%. В сульфитном щелоке содержится ряд кислот, некоторые из них являются летучими: уксусная (0,25—0,40%), муравьиная (0,04—0,08%), свободная сернистая (0,06—0,20%)- К летучим соединениям относятся также метиловый спирт (0,02—0,06%), фурфурол (0,03—0,06%), формальдегид (0,02—0,05%); общее количество летучих веществ, в сульфитном щелоке составляет 0,4—0,9%.
В состав сульфитного щелока входят также и нелетучие вещества. К ним относятся лигносульфоновые кислоты (3,5—5,5%), продукты разложения и окисления Сахаров: метилглиОксаль (0,05—0,07%), глицериновый альдегид, альдоновые кислоты и другие. Кроме перечисленных соединений, в сульфитном щелоке имеются минеральные соли сернистой, серной и других кислот, например бисульфит кальция в количестве 0,3—0,8%, моносульфит— 0,02—0,07%- Часть Сахаров щелока вступает в связь с сернистой кислотой, или бисульфитом, образуя альдегидбисуль — фитные соединения, не — сбраживаемые дрожжами. Тормозящее действие бисульфитных соединений на процесс брожения объясняется тем, что уксусный альдегид, образующийся в процессе спиртового брожения как промежуточный продукт, не превращается в дальнейшем в этиловый спирт, а дает с бисульфитом очень стойкое соединение, которое дрожжи не могут превратить в спирт. Если концентрация альдегидбисульфитных соединений в щелоке достигает 0,8%, то брожение практически прекращается. Кроме того, бисульфит и сернистая кислота угнетающе действуют на дрожжи, снижая их спиртообразующую способность.
Таким образом, вредные примеси гидролизатов и сульфитных щелоков так или иначе нарушают нормальные физиологические функции дрожжей и тем самым замедляют брожение. Кислотность щелоков жестких и мягких варок неодинакова; в первом случае рН достигает 1,9-н2,5; во втором рН = 2,5ч-3,5. Температура щелока, отобранного из котла, равна 80—95°.
На основании сказанного можно сделать вывод, что гидроли — заты и сульфитные щелока являются средами, мало пригодными для жизнедеятельности микроорганизмов по следующим причинам: 1) в этих средах в значительном количестве присутствуют различные вещества, угнетающие дрожжи (лигниновые и гуми — новые коллоиды, формальдегид, муравьиная кислота, фурфурол и его гомологи, продукты расщепления смолистых веществ, сернистый ангидрид и др.); 2) отсутствуют витамины и витамино — подобные вещества; 3) отсутствуют легкоусваиваемые соединения азота и недостаточно фосфорных соединений.
Для того чтобы эти среды были более благоприятными и полноценными, чтобы дрожжи наиболее эффективно сбраживали древесный сахар на спирт, необходимо создать им оптимальные условия развития:
• 1. Удалить вредные для дрожжей примеси. Серную кислоту и большую часть органических кислот нейтрализуют и этим уничтожают их токсическое действие на дрожжи. Для осуществления нормального процесса брожения рН среды должен быть оптимальным и равным для древесных гидролизатов 4,2—4,5; для сульфитных щелоков — мягких 4,8—5,2 и жестких 4,9—5,5; Для сбраживания гидролизатов, полученных из сельскохозяйственных отходов, рН сусла должен быть более низким (3,8—4,0), чем для древесных сусел, так как они легко заражаются посторонними микроорганизмами. Кислотность питательной среды в значительной степени влияет на деятельность ферментов дрожжей и на состояние их клеток, состоящих в основном из коллоидных веществ.
Летучие ядовитые вещества (фурфурол, терпены, сернистый ангидрид и др.) в основном удаляются со сдувочными парами, или с парами самоиспарения гидролизата, при продувке сульфитного щелока паром или воздухом. Часть фурфурола восстанавливается дрожжами в фурфуриловый спирт. Альдегидбисульфит — ные соединения разрушаются при удалении сернистой кислоты нейтрализацией или продувкой щелока воздухом.
В гидролизных средах остаются незначительные количества указанных выше летучих веществ, которые практически не влияют на спиртообразование. Так, не влияет на процесс образования спирта фурфурол при концентрации 0,05%’, уксусная кислота — 0,2%; S02 — 0,005% и бисульфит —0,03%.
Часть коллоиднорастворенных веществ гидролизатов коагулирует при нейтрализации и во время охлаждения нейтрализата; часть их адсорбируется активированным углем или коагулирует при действии различных химических реагентов, а также вместе с загрязнениями и взвешенными частицами отделяется при отстое и фильтрации. Соли тяжелых металлов в определенных концентрациях также тормозят брожение. Например, при концентрациях солей меди выше 0,004% брожение прекращается. Таким образом, несмотря на то, что в ходе технологического процесса большую часть вредных примесей гидролизных сред обезвреживают, некоторое количество их остается в сусле, Дрожжи постепенно привыкают к этим неблагоприятным питательным средам, изменяют свои свойства, вырабатывают новые ферменты и качества.
2. Для развития спиртообразующих дрожжей и для построения их ферментных систем в древесных и сульфитных суслах необходимо присутствие активаторов роста оргайической природы (витамины, витаминоподобные вещества), которые дрожжи самостоятельно синтезировать не могут. Источниками их являются экстракты солодовых ростков, дрожжевой автолизат, дрожжевая вода, причем, по данным М. Я. Калюжного, обработка ослабевших дрожжей дрожжевой водой способствует увеличению выходов спирта.
3. Поскольку в гидролизном и сульфитном сусле содержится недостаточное количество минеральных соединений азота и фосфора, его следует обогащать питательными солями — сульфатом аммония и суперфосфатом. Без добавления этих солей скорость сбраживания сахара снижается в 2—3 раза и увеличивается количество мертвых дрожжевых клеток.
Для стимулирования жизнедеятельности ослабленных дрожжей пользуются также методом фосфатной активации, т. е.’обра — батывают дрожжи суперфосфатной вытяжкой более высокой концентрации.
4. Брожение и размножение дрожжей зависит и от температуры среды. Оптимальная температура для этих процессов 30—33°. Более низкая температура замедляет скорость брожения и создает условия для развития посторонней инфекции. При замораживании дрожжи не погибают, только временно приостанавливаются их жизненные процессы, которые возобновляются вновь, если замерзшие дрожжи медленно оттаивать при 5—7°. При температуре сусл’а, равной 35—36°, скорость брожения повышается, но тормозится размножение, наступает угнетение
|
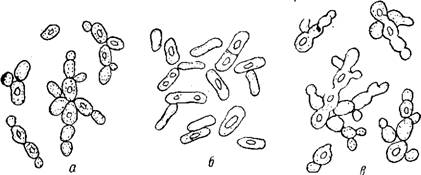
Рис. 137. Спиртообразующие гидролизные дрожжи: А — Saccharomyces cerevlslae; 6 — Schizosaccharomyces Pombe; В — Saccharomyces uvarum |
Дрожжей и постепенное их отмирание. При более высоких температурах (45—55°) наступает автолиз дрожжей. Следовательно, гидролизаты и сульфитные щелока необходимо охлаждать.
5. Для лучшего размножения, а также активации ослабленных дрожжей необходима аэрация питательной среды, так как построение веществ протоплазмы новых молодых клеток связано с затратой энергии, получаемой дрожжами в процессе дыхания. Поэтому небольшое количество воздуха подают, обычно в начале брожения. Процесс же спиртового брожения происходит в анаэробных условиях, и необходимую для жизнедеятельности энергию дрожжи получают в процессе брожения.
Таким образом, в результате соответствующей подготовки гидролизаты и сульфитные щелоки становятся благоприятной питательной средой для жизнедеятельности дрожжей, которые с полной эффективностью используют сахара этих сред и превращают их в ценные продукты.
Спиртообразующие дрожжи, применяемые в гидролизной промышленности, относятся к родам Saccharomyces, и Schizosaccharomyces и в основном к видам Saccharomyces cerevisiae, S. vini var. cartilaginosus, S. paradoxus, S. uvarum, Schizosaccharomyces Pombe и др. (рис. 137). На большинстве гидролизных заводов в настоящее время используют ветвистые дрожжи. На некоторых заводах преобладают пылевидные дрожжи (Бобруйский завод), а на нескольких — шизосахаромицеты.
В табл. 53 кратко дана биохимическая и физиологическая характеристика некоторых производственных дрожжей спиртового брожения, применяемых на гидролизных заводах (по данным Т. Н. Семушиной).
Таблица 53
|
Биохимическая и физиологическая характеристика дрожжей
|
Данные, приведенные в таблице, получены при сбраживании синтетических сред заводскими культурами дрожжей. Выход спирта на производственных средах несколько ниже и колеблется в пределах 53—55,5 л со 100 кг сброженного сахара.
Наиболее активными расами гидролизных дрожжей, производящими энергичное брожение, в настоящее время являются следующие культуры сахароминцетов: ленинградская Л-С-1, тав — динская Т-С-1, ферганская Ф-C-I и хакасская Хак-C-I. Наиболее полно и активно сбраживают галактозу штаммы: ЛОБ-С-1; Т-С-2, Т-С-3, ХАК-С-1. В последние годы наиболее широко распростра — • нены шизосахаромицеты.
На некоторых гидролизных заводах (Канском, Косьвинском, Хорском и др.) были обнаружены и выделены шизосахаромицеты, полнее сбраживающие сахара и дающие на 7—9% больше спирта, ;чем сахаромицеты. Температура брожения их 35—36°, но они име|ют и недостатки: нестойки при хранении и медленно размножаются; при специальных режимах шизосахаромицеты можно сохранять. Среди различных видов шизосахаромицетов наи-
|
|
|
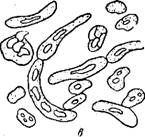
Рис. 138. Сорбирующиеся культуры дрожжей: А—Приозерская-4 (род Saccharomyces) б—Неманская-2 (род Zygofabospora); В — Суханская-7 (род Fabospora) ; |
|
© |
Более устойчивыми являются дрожжи Schizosaccharomyces Pom — be штамм К-К (канская-копулирующая). Наибольший выход спирта дают шизосахаромицеты Косьвинского и Архангельского заводов (КОС-С-1 и А-С-1). Описанные расы выделены как наиболее эффективные и высокопродуктивные из микрофлоры гидролизных заводов. Культуры дрожжей, приспособленные к условиям данного производства, применяемые длительное время и дающие в этих условиях хороший выход необходимых продуктов, называются местными расами дрожжей.
На большинстве сульфитно-спиртовых заводов применяются культуры сорбирующихся дрожжей, т. е. прикрепленных к волокнам целлюлозы.
К сорбирующимся дрожжам (рис. 138) относятся представители различных родов и видов семейства сахаромицетов. В основном они представлены родами: Saccharomyces, Fabospora и Zygofabospora. Краткая биохимическая и физиологическая характеристика некоторых сорбирующихся дрожжей приведена в табл. 54 (По данным М. Я. Калюжного).
|
545 |
Наиболее активными спиртообразующими дрожжами являются следующие местные культуры: П-4, Св-1, Б-7, Н-2, Св-20,
35 а. к. Славянский
|
Выход |
|||||
|
Спирта в л |
|||||
|
На 100 кг |
|||||
|
Завод |
Шифр культуры |
Видовое название |
Морфологические признаки |
Сбраживаемые сахара |
Общих РВ при сбраживании щелоков Приозер — ского завода |
|
Таблица 54 |
|
Биохимическая и физиологическая характеристика сорбирующихся дрожжей |
|
Приозерский |
|
П-4 |
|
Saccharomyces Vinl |
|
Зернистая |
|
Глюкоза, сахароЗа, мальтоза, манноза, слабо галактоза |
|
Св-1 С в-20 К-2 Б-7 СХ-7/ Н-2 |
Светогор — ский
Клайпедский
Балахнин — ский
Сухонский
Неманский
То же
Saccharomyces paradoxus
Saccharomyces vinl var. car — tllaginosus
To же
Fabospora fra — gllis
Zygofabospora marxlana
To же
Пылевидная
Зернистая
To же
Пылевидная
То же
То же
Глюкоза, манноЗа, сахароза, галактоза
Галактоза, глюкоза, сахароза, мальтоза
То же
Глюкоза, манноЗа, сахароза, галактоза, лактоза
|
44,5 43,4 |
|
43,0 41,7 42,4 41,0 42,2 |
То же
Но последняя слабо сорбируется. Выход спирта в заводских условиях меньше, чем приведенный в таблице. Сорбирующиеся дрожжи К-2, Б-7, СХ-7, Н-2, Св-20 и др. наряду с другими сахарами хорошо сбраживают галактозу. Это так называемые галактозные дрожжи, содержащие фермент галактозимазу.
При помощи так называемой проточной камеры, изобретенной М. Я — Калюжным, было показано, что дрожжи, сорбированные на волокнах, размножаются в 2 раза быстрее, чем находящиеся в жидкости. Таким образом, на границе твердая фаза — жидкость процессы размножения дрожжей протекают более активно, чем в жидкой фазе.
На выход спирта или скорость его образования, а также на физиологическое состояние дрожжей большое влияние оказывает концентрация дрожжей в бражке. Она должна соответствовать количеству питательных веществ в бражке, которые обеспечили бы и прирост молодых клеток и стойкость зрелых. Лучшая концентрация — 15—20 г дрожжей в 1 л, это количество дрожжей быстро сбраживает сахар, обычно в течение 6—7 часов, и выход
^спирта достигает 54 л со 100 кг сбраживаемых Сахаров. Такая концентрация обеспечивает и необходимый прирост дрожжей, так как при высокой концентрации дрожжи медленно размножаются, постепенно отмирают, и брожение замедляется* а при малой — дрожжи так активно размножаются, что часть сахара используется на этот процесс, и, следовательно, выход спирта понижается.
Концентрация и природа сахара также влияют на скорость брожения. На основании многих исследований можно сделать вывод, что при концентрации сбраживаемого сахара, равной 1,5—4%, древесное и сульфитное сусло сбраживается с максимальной скоростью. Если концентрация сахара упадет ниже 1%, скорость брожения быстро замедляется. Повышение концентрации сахара выше 15% отрицательно влияет на дрожжи, нарушая их обмен веществ, а высокая концентрация спирта парализует деятельность ферментов. Скорость брожения зависит также ог природы Сахаров. Наиболее быстро сбраживаются глюкоза и фруктоза, медленнее манноза и совсем медленно галактоза.
Для эффективной жизнедеятельности дрожжам необходимы питательные вещества. Вопросы питания микроорганизмов, в частности дрожжей, были рассмотрены в главе 30. Отметим только некоторые особенности питания гидролизных дрожжей. Углеродным питанием их являются шестиатомные сахара, входящие в состав гидролизатов и сульфитных щелоков: глюкоза, манноза, фруктоза и галактоза. Хуже усваиваются органические кислоты, например уксусная. В качестве азотистого питания дрожжи используют аммиачные соли (сульфатаммония); а ослабленные дрожжи — дрожжевой автолизат и дрожжевую воду, содержащие витамины и продукты распада белков дрожжевой клетки (аминокислоты и др.). Для дрожжей необходимо и минеральное питание, значение которого уже отмечалось. Фосфор вводят в среду в виде суперфосфата. Калий, натрий, кальций, магний, сера, хлор, бром и другие элементы переходят в раствор в виде солей из производственной воды и растительной ткани при ее гидролизе. Некоторые элементы: железо, медь, марганец, молибден, цинк, кобальт, хром, никель, теллур, необходимые для жизненных процессов дрожжей в небольших количествах, попадают в сусло в результате коррозии металлической аппаратуры.

 Опубликовано в рубрике
Опубликовано в рубрике