|
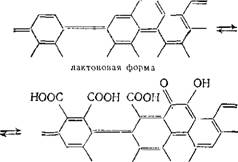
И кислотных поверхностных оксидов: |
|
О о ОН ( Ноос соон > / | / W |
|
|
|
О ОН |
|
,ОН |
|
Открытая форма |
В процессе окисления обеззоленного активного угля кислородом с ростом температуры постепенно возрастает поглощение кислорода, сопровождающееся повышением способности активного угля нейтрализовать основания [20, 21]. Напротив, при постепенном нагревании окисленных углей в определенных температурных интервалах происходит выделение ди — или мо — ноксида углерода, сопровождающееся восстановлением кислого характера поверхности. Пури [21] и Бартон [22] в многочисленных опытах показали присутствие определенных «комплексов», которые, в зависимости от продуктов разложения, получили название «СО-комплексов» или «СОг-комплексов». Одновременное измерение кислотных свойств позволило, например, идентифицировать разлагающийся примерно при 200 °С С02- комплекс как одновалентную слабую кислоту. Наряду с химическими свойствами поверхности, характер и концентрация поверхностных оксидов влияют на адсорбционное поведение активных углей. Можно показать, что С02-комплекс определяет полярные свойства, которые повышают сорбциониую способность относительно метанола. СО-комплекс способствует увеличению адсорбции бензола. Кислые поверхностные оксиды придают активному углю гидрофильные свойства, которые проявляются в повышенной способности поглощать пары воды при низких парциальных давлениях и увеличении теплоты смачивания водой [23]. При окислении активных углей в водном растворе хлором в условиях, типичных для дехлорирования сильно хлорированной воды, наблюдается определенное повышение концентрации кислых поверхностных оксидов, сопровождающееся снижением адсорбционной способности по отношению к различным органическим веществам [24]. Кюн и Зонт — хаймер [25] исследовали 5 промышленных активных углей и
заметили изменение адсорбционных свойств после воздействия озоном или перманганатом калия в процессе водоподготовки. С повышением значения рН окисленных углей наблюдается снижение адсорбционной способности по отношению к фенолу, ацетилсалициловой кислоте и резорцину. Перманганат калия оказывает более вредное действие по сравнению с озоном.
Интересно отметить влияние солей, образованных щелочными или щелочноземельными металлами с кислотными поверхностными оксидами, на адсорбцию водяного пара. Если у окисленного сахарного угля нейтрализовать возможно большую часть ионов водорода (~440 мг-экв/100 г угля по отношению к исходным 675 мг-экв/100 г), то оказывается, что на поглощение водяного пара особенно сильно влияют соли щелочных металлов (табл. 2.1).
|
ТАБЛИЦА 2.1. Поглощение водяного пара (масс. %) сахарными углями, у которых кислые поверхностные оксиды нейтрализованы различными основаниями (по данным Пури [25])
|
|
2.2.4. Серусодержащие поверхностные соединения |
Обеззоленные активные угли поглощают различные количества серы при нагревании в присутствии элементарной серы и различных ее соединений, например, сероводорода, сероуглерода или диоксида серы [26]. При этом сероводород поглощается в меньших количествах в сравнении с другими реагентами. Также отмечается определенная зависимость поглощения серы от содержания кислорода и особенно водорода в исходном угле. Вероятно, поглощенная сера входит в состав присутствующих на поверхности оксидов, причем в результате обменной реакции с S02 образуются преимущественно сульфоновые и сульфоксидные группы. В присутствии серы и сероводорода образуются сульфидные и гидросульфидные группы. При этом известно, что такие содержащие серу активные угли способствуют катализируемой сульфидными ионами реакции замещения азидов на иод с образованием иодида и азота. На прокаленных, свободных от кислорода и водорода активных углях сера образует С—S—С-группы на ненасыщенных центрах решетки.
Это ведет к заметному сужению пор, на что указывают изотермы адсорбции паров воды, бензола или метанола.
В определенных технических процессах, например в процессе «Сульфрин», описанные выше эффекты приобретают практическое значение, так как соединения серы в большинстве случаев оказывают сильное вредное действие на свойства угля. Образование необратимых соединений серы и связанную с этим потерю активности угля можно предотвратить блокированием активных центров, например, щелочным силикатом [27].

 Опубликовано в рубрике
Опубликовано в рубрике