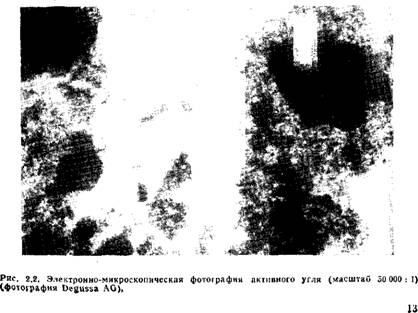
В первые десятилетия нашего века активный уголь обычно принимали за аморфную разновидность углерода. Хотя электронные микрофотографии позволяют различать рыхлую структуру, состоящую из мельчайших углеродных частиц размером около 3 нм, только рентгеноструктурный анализ Гофманна [1, 2] впервые показал, что эти частицы представляют собой кристаллиты размерами 1—3 нм. Поэтому в настоящее время активный уголь относят к группе микрокристаллических разновидностей углерода. Хотя графитовые кристаллиты состоят из плоскостей протяженностью 2—3 нм, образованных шести — членными кольцами, типичная для графита ориентация отдельных плоскостей решетки относительно друг друга нарушена. Это означает, что в активных углях слои беспорядочно сдвинуты относительно друг друга и не совпадают в направлении, перпендикулярном плоскости слоев (рис. 2.1). Расстояние между слоями больше, чем у графита (0,3354 нм) и составляет от 0,344 до 0,365 нм. Диаметр заключенного в одной плоскости строительного элемента составляет 2,0—2,5 нм, а иногда и больше. Высота пачки слоев равна 1,0—1,3 нм. Таким образом, графитовые кристаллиты в активном угле содержат 3— 4 параллельных углеродных слоя.
Химическим подтверждением графитной структуры активных углей является возможность образования соединений внедрения; так, Фреденхагену [3] удалось получить соединения Щелочного металла с графитом, а Руфф [4] получил фторированный графит.
Вследствие присутствия упорядоченной графитной структуры активные угли обычно характеризуются заметной электрической проводимостью. Отчасти она зависит от температуры
Рис. 2.1. Структура графитовых слоев:
А — упорядоченная структура в графите; б—неупорядоченная структура в микрокристаллическом углероде (активном угле).
Активирования и возрастает при высоких температурах, так как при этом удаляются действующие в качестве изоляторов поверхностные кислородные соединения (см. раздел 2.2) и образуются более крупные элементарные кристаллиты [5].
Ниже показано влияние продолжительности т и температуры прокаливания T на удельное объемное электрическое сопро тивление р древесного угля (букового ретортного):
|
U ч |
— |
3 |
3 |
3 |
18 |
|
Т, °С |
— |
500 |
550 |
600 |
600 |
|
Ру, Ом • см |
> 106 |
> 10е |
5,5 • 105 |
3,82 |
44 |
|
T, ч |
3 |
18 |
3 |
18 |
3 |
|
Т, °С |
700 |
700 |
800 |
800 |
900 |
|
Ру, Ом • см |
0,75 |
0,19 |
0,27 |
0,12 |
0,11 |
При высоких температурах, соответствующих температурам получения активного угля, удельное сопротивление на много порядков ниже чем при 400—500 °С. Прокаленные образцы измельчались в порошок и испытывались под давлением 18МПа в виде прессованных изделий.
Кроме графитовых кристаллитов активные угли содержат, по данным рентгеновского анализа Райли [6], от одной до двух третей аморфного углерода; наряду с этим присутствуют гете — роатомы, в частности, кислород. В углях, полученных из сырья, богатого кислородом, содержание последнего также очень высокое.
Неоднородная масса, состоящая из кристаллитов графита и аморфного углерода, обусловливает необычную структуру активных углей. Между отдельными частицами появляются щели и трещины (поры) шириной порядка Ю~10—10~8 м. Эти промежуточные поры прежде называли «микропорами» [7], а большие полости с диаметром до 1 мкм — «макропорами». Через эту систему пор осуществляется массопередача во всех процессах, протекающих на внутренней поверхности углерод- содержащего материала. Полости, не сообщающиеся с внешней поверхностью, называются «криптопорами». С точки зрения адсорбционной практики они не имеют никакого значения.
Принятое вначале деление на микро — и макропоры оказалось слишком грубым для описайия адсорбционных процессов. Поэтому Дубинин [8] предложил следующую классификацию пор: микро-, переходные и макропоры. В соответствии с этим делением микропоры представляют собой тончайшие поры, которые заполняются адсорбтом при низких парциальных давлениях, еще до капиллярной конденсации (см. раздел 3.4). Переходными являются поры, в которых имеет место капиллярная конденсация, а макропоры имеют настолько большие радиусы, что явление капиллярной конденсации уже становится невозможным.
В настоящее время такая классификация — преимущественно ее аналитико-технические аспекты — приведена в соответствие с нормами Международного союза чистой и прикладной химии (IUPAC) [9]. Поры с диаметрами до 0,4 нм называются субмикропорами, поры с диаметрами в интервале 0,4—
|
|
Рис. 2.3. Снимки, полученные с помощью растрового электронного микроскопа угля нз древесины бука, активированного водяном паром в масштабе 1000 : 1 (а), 3000:1(6), 10 000 : 1 (в),10 000 : 1 (г).
2,0 нм — микропорами. Для пор с диаметрами от 2 до 50 нм предлагается название мезопоры, более крупные поры с диаметрами выше 50 нм называются макропорами.
Пользуясь представлениями о диаметрах или радиусах пор, которые следует рассматривать как эффективные параметры, можно допустить, что поры имеют только цилиндрическую форму. Однако в активных углях преобладают V-образные и щелевидные поры наряду с порами неправильной формы. В большинстве промышленных активных углей одновременно присутствуют поры различной формы. Кроме того, во многих исследованиях доказывается существование так называемых бутылкообразных пор с узкими входами, которые образуются, в частности, в классическом процессе хлорцинкового активирования.
Распределение пор по радиусам в отдельных активных углях может быть весьма различным. В соответствии с этим различают крупнопористые активные угли, которые, однако, всегда содержат тонкие поры, и тонкопористые активные угли,
Которые кроме микропор могут включать и крупные поры. Ниже приведено типичное распределение пор в активных углях (объем пор в мл/г):
Микропоры Мезопоры Макропоры D<2 нм 0 = 2-50 им £>>50 нм
TOC o "1-3" h z Активные угли, крупнопо- 0,1—0,2 0,6—0,8 0,4
Ристые
Активные угли, тонкопо — 0,6—0,8 0,1 0,3
Ристые
Активный кокс 0,1 0,1 0,1
Углеродное молекулярное 0,25 0,05 0,1
Сито
Активный кокс является специфическим продуктом, отличающимся особенно однородным распределением микропор. Углеродные молекулярные сита до сих пор не нашли широкого применения в адсорбционной технике, очевидно, из-за своей высокой стоимости.
В настоящее время еще невозможно получить оптическое изображение системы микропор активных углей. Даже при чрезвычайно сильном увеличении электронно-микроскопические снимки, показанные на рис. 2.2, позволяют различать только Поры с диаметром около 10 нм. Значительно меньшее увеличение дают снимки с помощью растрового электронного микроскопа, которые, однако, достаточно наглядно воспроизводят структуру поверхности частицы. На рис. 2.3 представлены снимки, полученные на древесном угле, активированном водяным паром. Еще отчетливо заметна структура растительных клеток, однако эти клеточные каналы нельзя смешивать с адсорбционными порами. Только на рис. 2,3, виг увеличение до 1 : 10000 позволяет наблюдать макропоры с диаметрами 50— 100 нм.
2.2. ХИМИЧЕСКИЕ СВОЙСТВА. ПОВЕРХНОСТНЫЕ ОКСИДЫ 2.2.1. Элементный анализ активных углей
При прокаливании активных углей на воздухе образуется более или менее значительный остаток, обычно называемый золой. Источником этих неорганических компонентов может служить исходный материал или оставшиеся после неполной отмывки активирующие добавки и катализаторы. Кроме того, элементный анализ показывает, что в углеродном скелете активного угля может присутствовать определенное количество инородных атомов. Ниже представлены данные типичного элементного анализа двух обеззоленных углей марок F и S:
С, % и, % о, % N, %
Активный уголь F 93,4 0,7 5,3 0,6
Активный уголь S 94,0 1,0 4,7 0,3
Исследованиями установлено, что эти инородные атомы химически связаны с углеродом. Из описания кристаллической структуры, приведенного выше, следует, что пакеты слоев содержат по краям углеродные атомы, имеющие ненасыщенные химические связи. Вследствие такого энергетического состояния «активных центров», к которым относятся также и дефекты кристаллической решетки, уже при сравнительно низких температурах происходят реакции обмена с кислородом и водородом из окружающей атмосферы. Реактивность активного угля проявляется в его способности поглощать при контакте с определенными веществами, наряду с кислородом и водородом, также и другие гетероатомы. Так, в контакте с газовой фазой, содержащей элементарный хлор, активные угли образуют го — меополярные соединения углерода с хлором [10]; при нагревании органические хлорсодержащие соединения разлагаются. Описаны также активные угли [11], которые после определенных процессов обессеривания (например, процесс «Сульфрин», см. раздел 6.5.4) содержат несколько процентов химически связанной серы; обычная десорбция серы экстрагированием или нагреванием в этом случае невозможна, и только деструктивная гидрогенизация обеспечивает превращение серы в летучий сероводород.
Кислородные комплексы микрокристаллического углерода, так называемые поверхностные оксиды, сильно влияют на полярные свойства углеродной поверхности и ее адсорбционную способность и поэтому привлекают постоянное внимание исследователей. Полярность поверхности активного угля, содержащей поверхностные кислородные соединения, обусловливает интенсивную адсорбцию паров воды из влажной газовой атмосферы, одновременно может замедляться поглощение других паров или газов. В жидкой фазе избирательная адсорбционная способность активных углей относительно различных полярных веществ зависит от этих поверхностных соединений. Следовательно, поверхностные кислородные соединения важны и с практической точки зрения.

 Опубликовано в рубрике
Опубликовано в рубрике