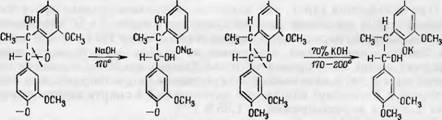
Даже непродолжительное воздействие щелочи на растительное сырье при повышенных температурах (160—170°) приводит к частичному растворению лигнина; раствор щелочи при этом приобретает желто-бурую окраску, которая далее постепенно усиливается до темно-коричневой. В производстве этот раствор поэтому и называют черным щелоком. При дальнейшем действии щелочи, в зависимости от времени обработки при высокой температуре, происходит более или менее полное удаление лигнина из растительного сырья.
При подкислении полученного черного щелока минеральной кислотой выпадает объемистый хлопьевидный осадок коричневого цвета, представляющий собой так называемый щелочной лигнин.
В 90 х годах прошлого столетия у первых исследователей щелочного лигнина, естественно, возникала мысль о его кислотном характере. Кла- сон, Ланге и другие ученые нредполаг али, что в разбавленных щелочах и в воде растворяются натриевые соли так называемых «лигниновых кислот», а при подкислении минеральными кислотами они разрушаются с выпадением в осадок.
Позднее (1910 г.) [70] было установлено, что частичное выпадение осадка лигнина наблюдается при нейтрализации черного щелока даже такой слабой кислотой, как угольная. Так как угольная кислота не способна вытеснять из солей даже самые слабые органические кислоты, то предположили, что лигнин взаимодействует со щелочью с образованием фенолятных соединений, способных легко разлагаться угольной кислотой
R—ОН + NaOH —>R—ONa + Н20; R—ONa + H2C03 —> R—ОН + NaHCOgi
*
Вещество, получаемое в результате подкисления черного щелока кислотами, ни в коей мере не может считаться неизмененным лигнином, поскольку варочный процесс проводился при высокой температуре. По мнению Гесса, например, измененные и загрязненные примесями лигнины. осажденные из натронных черных щелоков, вряд ли являются удобными объектами для изучения их структуры. Однако необходимость разъяснения процессов, происходящих при щелочных способах получения технической целлюлозы, побудили многочисленных исследователей заниматься изучением свойств щелочных лигнинов.
Щелочной лигнин не является строго индивидуальным веществом, а представляет смесь продуктов весьма родственного строения, притом отчасти изменяющихся при энергичном нагревании в щелочной среде. В течейие ряда лет Йн исследовался путем разделения его на фракции избирательным действием разных растворителей.’ Так, например, в одном из ранних исследований Холмберг и Винцель [[92]], занимавшиеся изучением лигнина, выделенного из черного щелока натронной варкой, разделили его по растворимости в спирте на две фракции (а — и у-щелочной лигнин). Первая из этих фракциГ оказалась нерастворимой в спирте, она содер
жала углерода на 1.2% меньше, чем вторая. Авторы пришли к заключению, что на каждую группу С40 в лигнине содержатся четыре метоксильные группы ОСН3. При метилировании этого лигнина (диметилсульфатом в присутствии щелочи) удавалось ввести в него еще два метоксила. Разное отношение осажденного из щелочного раствора лигнина к спирту и другим органическим растворителям можно отчасти объяснить неодинаковой степенью дисперсности коллоидных частиц. Незначительное различие в элементарном составе также может оказывать влияние на растворимость лигнинных фракций.
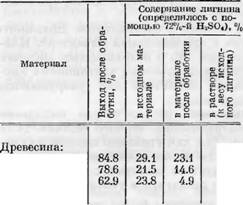
Легкость, с которой лигнин извлекается из растительного материала действием водных или спиртовых растворов щелочи, зависит от самой природы этого материала. В тех случаях, когда в качестве исходного материала берется солома хлебных злаков, стеблей и початков кукурузы, некоторые фракции лигнина могут быть извлечены действием водных или спиртовых растворов щелочи даже на холоду, в случае же, когда берется древесина, требуется более энергичная обработка при нагревании. Так, например, солома хлебных злаков по сравнению с лиственной и хвойной древесиной значительно легче отдает лигнин при обработке слабыми растворами щелочей. Опыты Розен — бергера [5], проведенные еще в 1933 г., показали, что при двухчасовой обработке 1%-м раствором NaOH при 95° ржаная солома отдает лигнин в 3V2—4 раза быстрее, чем древесина (табл. 186).
Бекман и Лише [в] выделяли лигнин из соломы озимой ржи путем длительной обработки холодной 1.5%-й водной щелочью или холодным 2%-м спиртовым раствором NaOH. В первом случае в раствор, кроме лигнина, переходила и некоторая часть гемицеллюлоз (их удаляли легким гидролизом горячей 2%-й НС1 или путем повторного осаждения спиртом), во втором случае — только лигнин. Полученные препараты лигнина содержали 62.5% С и 5.64% Н; кроме того — около 15.2% метоксильных групп, так что на каждые 10-11- атомов углерода приходилась одна метоксиль — ная группа. Так как при осторожном бензоилировании действием С6НБСОС1 на лигнин в присутствии NaOH или в присутствии пиридина на каждые 10—И атомов углерода вступала в реакцию I группа СвН5С0, то предполагалось, что в указанном комплексе лигнина содержится I группа ОН.
Жеребов и Малютин [7] выделяли лигнин из измельченной древесины ели мягким методом — обработкой водно-спиртовой щелочью при низкой температуре, и получали продукты, растворимые в органических растворителях: пиридине, хинолине, муравьиной и уксусной кислоте, водном спирте и ацетоне. В этом случае путем длительной обработки извлекалось 4/5 всего лигнина.
|
Таблица 186 |
|
I Результаты делигнификации древесины и ржаной соломы |
|
Осины. . . Ржаная солома |
|
20.8 31.9 79.2 |
Скорость растворения лигнина при обработке древесины, а также выделенного лигнина разбавленными растворами щелочей сильно зависит
от температуры раствора. Так, например, по данным Хегглунда, при действии на лигнин, выделенный из древесины 42%-й НС1 10%-м NaOH при 100° можно перевести в раствор в течение 2 час. всего лишь около 15% взятого вещества. Если температуру нагревания поднять до 170° и действовать даже более слабой щелочью, то за 3 часа можно перевести в раствор до 98% взятого лигнина. Н. Никитин и Орлова [8] указывают, что для процесса делигнификации опилок во время варки под давлением в закрытых котлах существенной является только температура, давление же практически не играет роли.
Действие растворов NaOH и КОН на лигнин при температурах 200° и выше сопровождается весьма значительным изменением лигнина, приводящим к повышению процента углерода в его составе. Однако, интенсивное отщепление его метоксильных групп с образованием метилового спирта по схеме
ROCHg + NaOH —* RONa + CH3OH
Происходит лишь при температурах, близких к 300°. Путем обработки лигнина, выделенного из древесины соляной кислотой, 4—5 н КОН при 300°, получается потемневший, не растворяющийся в щелочи остаток, элементарный состав которого по сравнению с исходным лигнином представлен в табл. 187.
|
Таблица 1S7 Элементарным состав продуктов нагрепания лигнина со щелочью
|
Нагревание того же лигнина с одной водой до 300° под давлением не влечет за собой отщепления метоксильных групп, однако изменяет его свойства. Кратцль [9] указывает, что с увеличением температуры нагревания древесины ели или выделенного из нее лигнина с водой выше 100° выход ванилина из них при окислении нитробензолом в щелочной среде снижается. Так, например, выход ванилина из древесины ели, предварительно нагревавшейся с водой при 200° в течение 20 час., составляет только 16% от ванилина, получающегося из исходной древесины. Термическая обработка древесины, а также изолированного лигнина с водой приводила, по мнению автора, к его конденсации в так называемый «трехмерный фенольный полимер» с высоким содержанием метоксильных групп, но не дающий ванилина при нитробензольном окислении. Нагревание с водой в тех же условиях кониферилового альдегида, в качестве модельного вещества, снижало выход из него ванилина с 64 до 49%; это указывало на относительно большую устойчивость к конденсации кониферилового альдегида по сравнению с лигнином. Гольдшмид [10] изучал перешедшие в раствор продукты нагревания древесной муки западного хемлока (Tsuga Heterophylla) с водой при 175° в течение 45 мин. путем их фракционирования эфиром и бисульфитом натрия. В растворимой в бисульфите фракции, извлеченной из эфирного раствора, им было обнаружено путем хроматографии на бумаге присутствие п-кумарилальдегада, ванилина, кониферилового альдегида, ванилоилметилкетона и гваяцил — ацетона. Подобный водный гидролиз нативного лигннна Браунса из хемлока также давал указанные продукты, причем выход кониферилового альдегида из объединенных эфирных экстрактов двух последующих гидролизов составлял около 3—4% от нативного лигнина.
В одном из ранних исследований было показано, что только часть лигнина осаждается кислотами из черного щелока натронной варки. Другая же часть его, приблизительно 7% к весу древесины, оставалась при подкислении в растворе и была названа Хегглундом «воднораство — римым лигнином». При дальнейшем исследовании этой части лигнина Эн — квист [и] показал, что она состоит из трех фракций, каждая из которых составляет около 2% к весу исходной древесины. Первая фракция, растворяющаяся уже около 100°, при нормальной натронной и сульфатной варках имеет низкое содержание метоксильных групп и ультрафиолетовый спектр поглощения, отличающийся от спектра лигнина. Вторая фракция содержит продукты разрушения лигнина неароматической природы. Третья же фракция состоит из продуктов превращения лигнина, образующихся главным образом при максимальных температурах варки (160— 180°), и содержит, по-видимому, днмеры фенилпропановых единиц, небольшие количества ванилиновой кислоты и простые метоксилсодержащие кетоны, такие, как ацетогваякон. При нагревании натронного или сульфатного елового лигнина с NaOH при температурах около 170° от 7 до 26 % лигнина может превращаться в продукты, почти идентичные с третьей фракцией. В двухступенчатой сульфатной варке при 110° и 167°, в условиях дальнейшего нагревания полученных лигнинов с NaOH, около 35% их превращается в эфирнорастворимые фенольные продукты.[93]
Хроматографическим разделением подобных продуктов превращения лигнина от двухступенчатых варок экстрагированной ацетоном еловой древесины (отдельно с NaOH и NaSH, по 6 час. при 100° и 170°) было показано [12], что перешедшие в раствор во второй ступени варки вещества содержали изоэвгенол, а-оксипропиогваякол, ванилин, ацетогваякон, гваякол, ванилилдисульфид и большое число неизвестных фенольных веществ. По ультрафиолетовым спектрам поглощения последних было установлено, что неизвестные фенольные вещества, полученные от варок с NaOH, отличались от соединений, полученных при варках с NaSH.
Гибберт с сотрудниками [13] еще в 1935 г. нашли, что минеральные кислоты осаждают из черного щелока после варки ели два различных препарата лигнина: «щелочной лигнин А», нерастворимый в смеси диоксана с эфиром, и «щелочной лигнин Б» — хорошо растворяющийся в этой смеси. Соотношение лигнинов А и Б в щелоке составляло приблизительно 4:1. Определяя свободные кислые гидроксильные группы в этих лигнинах путем ряда последовательных операций метилирования диазометаном, ацетилирования уксусным ангидридом в среде пиридина и полного метилирования диметилсульфатом в щелочной среде, авторы установили, что в процессе щелочной варки в лигнине возникают новые кислые (фенольные) гидроксильные группы [14]. По данным Фрейденберга, осторожно выделенный из древесины так называемый медноаммиачный лигнин содержит очень малое количество свободных фенольных гидроксильных групп. Образование их во время щелочной варки возможно, во-первых, за счет частичного гидролиза метоксильных групп под воздействием щелочи при высокой температуре с одновременным образованием метилового спирта.
Действительно, при щелочной варке получается около 0.7% метанола (11—13 кг на 1 т целлюлозы), удаляемого из котла сдувочными газами. В природном лигнине хвойных пород древесины в среднем содержится 16—17% метоксильных групп, а в щелочном лигнине их находят только около 13.5%. Разница в содержании метоксильных групп в природном и щелочном лигнинах близко соответствует практическому выходу метанола при щелочной варке. Приближенно можно сказать, что уменьшение содержания метоксилов в процессе щелочной варки отвечает одной метоксильной группе на единицу лигнина с молекулярным весом 850 [16].
Второй возможностью образования новых фенольных гидроксилов является расщепление кислородных гетероцпклов лигнина (фурановых или пирановых колец) по схеме I.
I I
|
Схема I Схема II |
Эта реакция была доказана Фрейденбергом на синтетическом модельном веществе — кислоте Эрдтмана. При сплавлении ее с 70%-й щелочью идет расщепление фуранового кольца и освобождение фенольного гидроксила по схеме II [16]. Разрыв кислородных гетероцпклов может частично происходить не только при сплавлении лигнина со щелочью, но и при варке с разбавленными щелочными растворами в условиях высокой температуры [17J.
Возможно, что процесс образования фенольных гидроксильных групп идет за счет комбинирования обеих реакций. Как первая реакция гидролиза метоксильных групп, так и вторая реакция расщепления кислородных гетероцпклов лигнина, вероятно, проходят постепенно и далеко не полностью. В результате образования повышающих растворимость лигнина солеобразных фенолятных групп сложный комплекс лигнина постепенно переходит в раствор.
Не вызывает сомнения, что при высокой температуре щелочной варки также происходит расщепление химических связей между лигнином и углеводами. Это тоже облегчает переход лигнина в раствор наряду с пеп- тизирующим действием образующихся фенолятных групп.
Характерно, что по вышеприведенной схеме I горячие растворы щелочей гидролизуют кислородные связи в а-положении боковых цепей лигнина по месту его бензильной группировки, представляющей собой простой эфир замещенного бензилового спирта. В результате гидролиза простой эфирной связи в этом месте и образуется весьма реакционноспособ — ный свободный спиртовой гидроксил, путем обмена которого и происходят такие важные реакции лигнина, как замещение на группы S03H при сульфитной варке, замещение на группы ОС2Н5 при этанолизе древесины и другие процессы. Поэтому в последнее время очень часто для разъяснения реакций лигнина при щелочных варках используется в качестве модельного вещества бензиловый спирт и в особенности ванплило — вый спирт.
TOC o "1-3" h z СН—О СН2ОН СН2ОН
У�СН3 уосн3
Еензильная группи — Бензиловый Ванилиловый
Ровна лигнина спирт спирт
При сульфатной варке, как известно, в варочном щелоке присутствует около 25—30% от общей щелочи сульфида натрия Na2S, переходящего при гидролизе в гидросульфид натрия NaSH. Еще в 1911 г. было найдено, что лигнин, осаждаемый кислотами из сульфатного черного щелока, содержит около 2.5% органически связанной серы [18]. Определяя содержание серы в двух лигнинах, различавшихся по растворимости в спирте, Андерсен и Хольмберг нашли, что растворимый в спирте лигнин содержал серы 2.5%, а нерастворимый — 1.95% [19].
Позднее, в 1941 г., Хегглунд показал [20], что количество серы, связанной с лигнином, зависит от сульфидности варочного щелока и увеличивается с повышением содержания Na2S в растворе. Проведя чисто натронные и сульфатные варки, а также варки с одним гидросульфидом натрия, Хегглунд получил осажденные из черного щелока лигнины с содержанием серы от 0 до 10%.
В 1948 г. при проведении двухступенчатых варок с водными растворами NaSH или H2S в первой ступени и с NaOH или пиридином — во второй Энквист [21] получил очень высокое содержание серы в лигнинах. Наиболее высокое содержание серы (до 17.5%) дали весьма длительные варки с водным раствором H2S в первой ступени и пиридином во второй.
При фракционировании сернистых лигнинов путем растворения в спирте, диоксане и эфире было найдено, что содержание серы в отдельных фракциях лигнина, даже одной и той же варки, весьма различно. В общем оно было ниже для фракций, растворимых в спирте, и выше — для растворимых в эфире.
Подробно исследуя свойства сернистых лигнинов, полученных в различных условиях, автор приходит к выводу, что лигнин в древесине уже при 100° и при почти нейтральной реакции способен присоединять серу в количествах, отвечающих примерно одному атому серы на одну фенилпро- пановую единицу7. Лигнин при этом переходит в форму, растворимую
не только в щелочи, но и в нейтральных растворителях (спирт, диоксан и др.).
Влияние температуры варки на количество органически связанной серы в лигнине, по данным Хенсона, характеризуется следующей кривой (см. рис. 165).
|
12 10 |
|
|
|
11 И «ё | ^ § |
|
110 120 130 140 150 160 170 180 С Температура. Варки Рис. 165. Зависимость содержания серы в лигнине от температуры сульфатной варки. |
На основании этой кривой автор [22] делает вывод, что в области низких температур содержание серы в растворенном лигнине ассимптотп — чески стремится к величине, равной примерно 3.6% серы и отвечающей приблизительно одному атому серы на четыре фенилпропановых единицы. Понижение содержания серы в лигнине при температурах варки свыше 160°, по предположению автора, возможно, обусловливается разрушением сернистых лигнинов с выделением серы при продолжительном воздействии щелочи и высокой температуры. Это предположение подтвердилось позднейшими исследованиями Энквиста [21> 23 ], показавшими, что если сернистый лигнин (полученный с H2S при рН=7 и 100° С) варить с 4%-м раствором NaOH в течение 3 час. при 160°, то содержание серы в лигнине падает с 8.45% до 4.1% с одновременным образованием значительных количеств гидросульфида натрия в растворе.[94] По-видимому, этим и объясняется низкое содержание серы (2.5—4.0%) в сернистых лигнинах, полученных при обычных сульфатных варках, даже с высокой сульфидноотыо варочного щелока.

 Опубликовано в рубрике
Опубликовано в рубрике